
题目列表(包括答案和解析)
实验室配制一定物质的量浓度的溶液时,需用到容量瓶,容量瓶是一种颈部细长的梨形瓶,由于其颈部细长,所以在向容量瓶中转移液体时,需一定的耐心和技巧,有人建议将容量瓶的瓶颈改粗,对该建议的正确评价是( )
| A.可以按此建议改进,便于使用容量瓶 |
| B.不能按此建议改进,因为会降低容量瓶的精度 |
| C.如果加粗瓶颈,可将原来刻在容量瓶瓶颈上的刻度改刻在容量瓶的瓶身上 |
| D.不必加粗瓶颈,因为向容量瓶中转移液体时,少量液体倒出瓶外,不会对溶液的浓度产生影响 |
| A.可以按此建议改进,便于使用容量瓶 |
| B.不能按此建议改进,因为会降低容量瓶的精度 |
| C.如果加粗瓶颈,可将原来刻在容量瓶瓶颈上的刻度改刻在容量瓶的瓶身上 |
| D.不必加粗瓶颈,因为向容量瓶中转移液体时,少量液体倒出瓶外,不会对溶液的浓度产生影响 |
现有下列物质:①NaCO3•10H2O晶体 ②铜 ③氯化氢 ④CO2 ⑤NaHSO4 固体 ⑥Ba(OH)2 固体 ⑦红褐色的氢氧化铁液体 ⑧氨水 ⑨稀硝酸 ⑩熔化的Al2(SO4)3
(1)按物质的分类方法填写表格的空白处:(填编号)
| 分类标准 | 能导电的物质 | 电解质 | 非电解质 |
| 属于该类的物质 |
(2)上述物质中有物质之间可发生离子反应:H++OH-![]() H2O,写出一个该离子反应对应的化学方程式 。
H2O,写出一个该离子反应对应的化学方程式 。
(3)⑩在水中的电离方程式为 ,17.1g⑩溶于水配成250mL溶液, SO42-的物质的量浓度为 。
(4)区别⑦和⑨的方法是 ,将⑨滴加到⑦中至过量的实验现象是
(5)②与⑨发生反应的化学方程式为: 2KMnO4 + 16HCl ══ 2KCl+2MnCl2+5Cl2↑+ 8H2O
上述反应的离子方程式 ,还原产物是 (填化学式)。
体现的盐酸的性质有 , 标况下生成3.36LCl2,转移电子的数目约为 ,被还原的盐酸的物质的量为 。
(6)向⑧中通入③至恰好完全反应,则⑧的导电能力的变化为
(7)将⑥的溶液滴加到⑤的溶液中至恰好沉淀为止时的离子方程式为 。
(8)用① 配制450mL 0.1 mol/L Na2CO3溶液,请回答下列问题:
a应用托盘天平称取Na2CO3·10H2O晶体______g。
b配制Na2CO3溶液时需用的主要仪器有托盘天平、烧杯、药匙、________、________、________。
c实验中下列情况会使所配溶液浓度偏低的是________
A.加水时超过刻度线 B.洗涤液未移入容量瓶
C.容量瓶内壁附有水珠而未干燥 D.定容时俯视刻度线
⑴有一学生在实验室测某溶液pH。实验时,他先用蒸馏水润湿pH试纸,然后用洁净干燥的玻璃棒蘸取试样进行检测。
①这种错误操作 (填“一定”/“一定不”/“不一定”)会导致实验结果有误差。
②若按此法分别测定c(H+)相等的盐酸和醋酸溶液的pH,误差较大的是 。
⑵、用已知浓度的 NaOH 溶液测定某 HCl溶液的浓度,参考右图,从表中选出正确序号 _____________
| 序号 | 锥形瓶中溶液 | 滴定管中溶液 | 选用指示剂 | 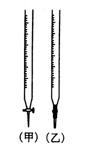 选用滴定管 选用滴定管 |
| A | 碱 | 酸 | 石芯 | (乙) |
| B | 酸 | 碱 | 酚酞 | (甲) |
| C | 碱 | 酸 | 甲基橙 | (甲) |
| D | 酸 | 碱 | 酚酞 | (乙) |
| 实验 编号 | 待测氢氧化钠溶液体积(mL) | 滴定开始读数(mL) | 滴定结束读数(mL) | 消耗盐酸体积(mL) |
| ① | 25.00 | 0.02 | 26.40 | |
| ② | 25.00 | 0.04 | 25.81 | |
| ③ | 25.00 | 0.03 | 25.78 | |
| ④ | 25.00 | 0.20 | 25.96 | |
⑴有一学生在实验室测某溶液pH。实验时,他先用蒸馏水润湿pH试纸,然后用洁净干燥的玻璃棒蘸取试样进行检测。
①这种错误操作 (填“一定”/“一定不”/“不一定”)会导致实验结果有误差。
②若按此法分别测定c(H+)相等的盐酸和醋酸溶液的pH,误差较大的是 。
⑵、用已知浓度的 NaOH 溶液测定某 HCl溶液的浓度,参考右图,从表中选出正确序号 _____________
|
序号 |
锥形瓶中溶液 |
滴定管中溶液 |
选用指示剂 |
|
|
A |
碱 |
酸 |
石芯 |
(乙) |
|
B |
酸 |
碱 |
酚酞 |
(甲) |
|
C |
碱 |
酸 |
甲基橙 |
(甲) |
|
D |
酸 |
碱 |
酚酞 |
(乙) |
⑶、用标准的NaOH滴定未知浓度的盐酸,选用酚酞为指示剂,造成测定结果偏高的原因可能是 。
A. 配制标准溶液的氢氧化钠中混有Na2CO3杂质
B. 滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C. 盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
D. 滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
E. 未用标准液润洗碱式滴定管
⑷、已知滴定管中装有浓度为0.112mol/L的盐酸。逐滴加入到装有氢氧化钠的溶液的锥形瓶中。开始时读数及恰好反应时盐酸的读数见下表。
|
实验 编号 |
待测氢氧化钠溶液体积(mL) |
滴定开始读数(mL) |
滴定结束读数(mL) |
消耗盐酸体积(mL) |
|
① |
25.00 |
0.02 |
26.40 |
|
|
② |
25.00 |
0.04 |
25.81 |
|
|
③ |
25.00 |
0.03 |
25.78 |
|
|
④ |
25.00 |
0.20 |
25.96 |
|
试计算待测的氢氧化钠的物质的量浓度= .
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com