(1)用NaCl固体配制100mL 1.00mol/L NaCl溶液的步骤为:计算;称量;溶解;洗涤;摇匀;装瓶贴签等.其中缺少的步骤名称有
移液、定容
移液、定容
.
(2)国际上规定,
0.012kg12C所含碳原子数
0.012kg12C所含碳原子数
叫做阿伏加德罗常数.
(3)在水溶液里或
熔融状态
熔融状态
下能够导电的
化合物
化合物
叫做电解质.
(4)酸、碱、盐在水溶液中发生的离子反应的条件是生成
沉淀、气体或弱电解质
沉淀、气体或弱电解质
,只要具备上述条件之一,反应就能发生.
(5)在化学反应中,如果反应前后元素化合价发生变化,就一定有
电子转移
电子转移
;元素化合价升高,该物质发生
氧化还原
氧化还原
反应.
(6)离子反应特有的守恒关系为
电荷
电荷
守恒;氧化还原反应特有的守恒关系为
电子转移
电子转移
守恒.
(7)将
饱和氯化铁溶液
饱和氯化铁溶液
滴入
沸水
沸水
中可制备氢氧化铁胶体,反应的化学方程式为
FeCl3+3H2O=Fe(OH)3(胶体)+3HCl
FeCl3+3H2O=Fe(OH)3(胶体)+3HCl
.

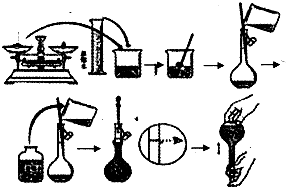 今欲用NaOH固体配制100mL 0.5mol/L的NaOH溶液.配制过程如图所示:
今欲用NaOH固体配制100mL 0.5mol/L的NaOH溶液.配制过程如图所示: