
题目列表(包括答案和解析)
以富含硫酸亚铁的工业废液为原料生产氧化铁的工艺如下(部分操作和条件略);
Ⅰ.从废液中提纯并结晶出FeSO4·7H2O.
Ⅱ.将FeSO4溶液与稍过量的NH4HCO3溶液混合,得到含FeCO3的浊液
Ⅳ.将浊液过滤,用90℃热水洗涤沉淀,干燥后得到FeCO3固体
Ⅴ.煅烧FeCO3,得到Fe2O3固体
已知:NH4HCO3在热水中分解
(1)Ⅰ中,加足量的铁屑除去废液中的Fe3+,该反应的离子方程式是_______
(2)Ⅱ中,生成FeCO3的离子方程式是________.若FeCO3浊液长时间暴露在空气中,会有部分固体表面变为红褐色,该变化的化学方程式是________.
(3)Ⅳ中,通过检验![]() 来判断沉淀是否洗涤干净.检验
来判断沉淀是否洗涤干净.检验![]() 操作是________
操作是________
(4)已知煅烧FeCO3的化学方程式是4FeCO3+O2![]() 2Fe2O3+4CO2,现煅烧464.0 kg的FeCO3,得到316.8 kg产品,若产品中杂质只有FeO,则该产品中Fe2O3的质量是________kg(摩尔质量/g·mol-1:FeCO3-116 Fe2O3-160 FeO-72)
2Fe2O3+4CO2,现煅烧464.0 kg的FeCO3,得到316.8 kg产品,若产品中杂质只有FeO,则该产品中Fe2O3的质量是________kg(摩尔质量/g·mol-1:FeCO3-116 Fe2O3-160 FeO-72)
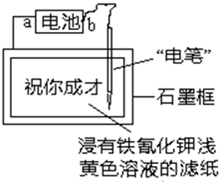 (2011?安庆三模)已知:含Fe2+的溶液与铁氰化钾K3[Fe(CN)6]溶液反应生成具有特征蓝色的铁氰化亚铁沉淀.现用如图装置在浸有铁氰化钾浅黄色溶液的滤纸上写出特征蓝色的字“祝你成才”.据此判断下列说法正确的是( )
(2011?安庆三模)已知:含Fe2+的溶液与铁氰化钾K3[Fe(CN)6]溶液反应生成具有特征蓝色的铁氰化亚铁沉淀.现用如图装置在浸有铁氰化钾浅黄色溶液的滤纸上写出特征蓝色的字“祝你成才”.据此判断下列说法正确的是( )| 充电 |
| 放电 |
| c(N2)c2(CO2) |
| c2(NO)c2(CO) |
| c(N2)c2(CO2) |
| c2(NO)c2(CO) |

 已知:3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓(蓝色).如图连接好装置,往铁电极区滴入2滴黄色的K3[Fe(CN)6](铁氰化钾)溶液.下列说法正确的是( )
已知:3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓(蓝色).如图连接好装置,往铁电极区滴入2滴黄色的K3[Fe(CN)6](铁氰化钾)溶液.下列说法正确的是( )| A | B |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com