
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
ЃЈ12ЗжЃЉЯТБэжаЫљСаЕФЪЧ8жжЖЬжмЦкдЊЫидзгЕФАыОЖМАжївЊЛЏКЯМлЃК
ЃЈ1ЃЉCдЊЫидкжмЦкБэжаЕФЮЛжУЮЊ Ёј ЃЛIE2ЕФЕчзгЪНЮЊ Ёј ЃЌGдЊЫизюЕЭМлЧтЛЏЮяЕФПеМфЙЙаЭЮЊ Ёј ЁЃ
ЃЈ2ЃЉBЁЂDЁЂEЫљДњБэдЊЫиЕФРызгАыОЖДгДѓЕНаЁЕФЫГађЮЊ Ёј ЃЈЬюРызгЗћКХЃЉЁЃGЁЂCзюИпМлбѕЛЏЮяЖдгІЫЎЛЏЮяЕФЫсадЧПШѕЙиЯЕЮЊЃЈаДЛЏбЇЪНЃЉ Ёј ЁЃ
ЃЈ3ЃЉCгыEаЮГЩЕФЛЏКЯЮяЪєгк Ёј ОЇЬхЁЃ
ЃЈ4ЃЉжмЦкБэжагааЉдЊЫиДцдкЁАЖдНЧЯпЯрЫЦЁБЯжЯѓЃЈвЛжждЊЫиЕФаджЪГЃЭЌЫќгвЯТЗНЯрСкЕФСэвЛжждЊЫиОпгаРрЫЦадЃЉЃЌЧыаДГіAЕФЕЅжЪгыЧПМюШмвКЗДгІЕФРызгЗНГЬЪНЃК Ёј ЁЃ
ЃЈ5ЃЉгаШЫШЯЮЊЃКHЁЊEМќЕФМќФмДѓгкHЁЊLМќЕФМќФмЃЌЫљвдH2EЕФЗаЕуИпгкH2LЕФЗаЕуЁЃФуЪЧЗёдоЭЌетжжЙлЕу Ёј ЃЈЬюЁАдоЭЌЁБЛђЁАВЛдоЭЌЁБЃЉ,РэгЩЃК Ёј ЁЃ
ЙЙГЩЮяжЪЕФЮЂСЃжжРрМАЯрЛЅМфЕФзїгУСІЪЧОіЖЈЮяжЪБэЯжГіКЮжжЮяРэаджЪЕФжївЊвђЫиЃЎ
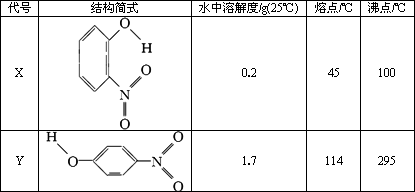
(1)Ш§ТШЛЏЬњГЃЮТЯТЮЊЙЬЬхЃЌШлЕу282ЁцЃЌЗаЕу315ЁцЃЌдк300ЁцвдЩЯвзЩ§ЛЊЃЎвзШмгкЫЎЃЌвВвзШмгкввУбЁЂБћЭЊЕШгаЛњШмМСЃЎОнДЫХаЖЯШ§ТШЛЏЬњОЇЬхжаДцдкЕФЮЂСЃМфзїгУСІга________ЃЎ
(2)ЧтМќзїгУГЃБэЪОЮЊЁАAЃHЁBЁБЃЌЦфжаAЁЂBЮЊЕчИКадКмЧПЕФвЛРрдзгЃЌШч________(СаОйШ§жж)ЃЎXЁЂYСНжжЮяжЪЕФЗжзгНсЙЙКЭВПЗжЮяРэаджЪШчЯТБэЃЌЖўепЮяРэаджЪгаВювьЕФжївЊдвђЪЧ________ЃЎ
(3)ИЦЪЧШЫЬхЫљашЕФживЊдЊЫижЎвЛЃЌгавЛжжВЙИЦМСЁЊЁЊПЙЛЕбЊЫсИЦЕФзщГЩЮЊCa(C6H7O6)2ЁЄ4H2OЃЌЦфНсЙЙЪОвтЭМШчЯТЃК
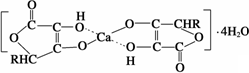
ИУЮяжЪжаДцдкЕФЛЏбЇМќРраЭАќРЈ________(ЬюзжФИ)ЃЎ
AЃЎН№ЪєМќ
BЃЎРызгМќ
CЃЎЗЧМЋадЙВМлМќ
DЃЎХфЮЛМќ
(4)ЂйCH2![]() CH2ЁЂЂкCHЁдCHЁЂЂл
CH2ЁЂЂкCHЁдCHЁЂЂл![]() ЁЂЂмHCHOЫФжжЗжзгОљФмгыH2ЗЂЩњМгГЩЗДгІЃЌМгГЩЪБетаЉЗжзгжаЗЂЩњЖЯСбЕФЙВМлМќЕФРраЭЪЧ________ЃЎетЫФжжЗжзгжаЬМдзгВЩШЁsp2дгЛЏЕФЪЧ________(ЬюађКХ)ЃЎ
ЁЂЂмHCHOЫФжжЗжзгОљФмгыH2ЗЂЩњМгГЩЗДгІЃЌМгГЩЪБетаЉЗжзгжаЗЂЩњЖЯСбЕФЙВМлМќЕФРраЭЪЧ________ЃЎетЫФжжЗжзгжаЬМдзгВЩШЁsp2дгЛЏЕФЪЧ________(ЬюађКХ)ЃЎ
 вбжЊAЁЂBЁЂCЁЂDЁЂEЖМЪЧдЊЫижмЦкБэжаЧАЫФжмЦкЕФдЊЫиЃЌЫќУЧЕФКЫЕчКЩЪ§AЃМBЃМCЃМDЃМEЃЎBдзгЕФpЙьЕРАыГфТњЃЌаЮГЩЕФЧтЛЏЮяЕФЗаЕуЪЧЭЌжїзхдЊЫиЕФЧтЛЏЮяжазюЕЭЕФЃЎDдзгЕУЕНвЛИіЕчзгКѓ3pЙьЕРШЋГфТњЃЎA+БШDдзгаЮГЩЕФРызгЩйвЛИіЕчзгВуЃЎCгыAаЮГЩA2CаЭРызгЛЏКЯЮяЃЎEЕФдзгађЪ§ЮЊ26ЃЌEдзгЛђРызгЭтЮЇгаНЯЖрФмСПЯрНќЕФПеЙьЕРЖјФмгывЛаЉЗжзгЛђРызгаЮГЩХфКЯЮяЃЎЧыИљОнвдЩЯЧщПіЃЌЛиД№ЯТСаЮЪЬтЃКЃЈД№ЬтЪБЃЌAЁЂBЁЂCЁЂDЁЂEгУЫљЖдгІЕФдЊЫиЗћКХБэЪОЃЉ
вбжЊAЁЂBЁЂCЁЂDЁЂEЖМЪЧдЊЫижмЦкБэжаЧАЫФжмЦкЕФдЊЫиЃЌЫќУЧЕФКЫЕчКЩЪ§AЃМBЃМCЃМDЃМEЃЎBдзгЕФpЙьЕРАыГфТњЃЌаЮГЩЕФЧтЛЏЮяЕФЗаЕуЪЧЭЌжїзхдЊЫиЕФЧтЛЏЮяжазюЕЭЕФЃЎDдзгЕУЕНвЛИіЕчзгКѓ3pЙьЕРШЋГфТњЃЎA+БШDдзгаЮГЩЕФРызгЩйвЛИіЕчзгВуЃЎCгыAаЮГЩA2CаЭРызгЛЏКЯЮяЃЎEЕФдзгађЪ§ЮЊ26ЃЌEдзгЛђРызгЭтЮЇгаНЯЖрФмСПЯрНќЕФПеЙьЕРЖјФмгывЛаЉЗжзгЛђРызгаЮГЩХфКЯЮяЃЎЧыИљОнвдЩЯЧщПіЃЌЛиД№ЯТСаЮЪЬтЃКЃЈД№ЬтЪБЃЌAЁЂBЁЂCЁЂDЁЂEгУЫљЖдгІЕФдЊЫиЗћКХБэЪОЃЉвбжЊAЁЂBЁЂCЁЂDЁЂEЖМЪЧдЊЫижмЦкБэжаЧАЫФжмЦкЕФдЊЫиЃЌЫќУЧЕФКЫЕчКЩЪ§AЃМBЃМCЃМDЃМEЁЃBдзгЕФpЙьЕРАыГфТњЃЌаЮГЩЕФЧтЛЏЮяЕФЗаЕуЪЧЭЌжїзхдЊЫиЕФЧтЛЏЮяжазюЕЭЕФЁЃDдзгЕУЕНвЛИіЕчзгКѓ3pЙьЕРШЋГфТњЁЃA+БШDдзгаЮГЩЕФРызгЩйвЛИіЕчзгВуЁЃCгыAаЮГЩA2CаЭРызгЛЏКЯЮяЁЃEЕФдзгађЪ§ЮЊ26ЃЌEдзгЛђРызгЭтЮЇгаНЯЖрФмСПЯрНќЕФПеЙьЕРЖјФмгывЛаЉЗжзгЛђРызгаЮГЩХфКЯЮяЁЃ
ЧыИљОнвдЩЯЧщПіЃЌЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉКЌгадЊЫиAЕФбЮЕФбцЩЋЗДгІЮЊ ЁЃаэЖрН№ЪєбЮЖМПЩвдЗЂЩњбцЩЋЗДгІЃЌЦфдвђЪЧ ЁЃ
ЃЈ2ЃЉCЕФЧтЛЏЮяЗжзгЕФМќНЧЪЧ ЃЌЪєгк ЗжзгЁЃЃЈЬюЁАМЋадЁБЛђЁАЗЧМЋадЁБЃЉ
ЃЈ3ЃЉBD3ЕФжааФдзгЕФдгЛЏРраЭЪЧ
ЃЈ4ЃЉEЕФвЛжжГЃМћХфКЯЮяE(CO)5ГЃЮТЯТГЪвКЬЌЃЌШлЕуЮЊ-20.5ЁцЃЌЗаЕуЮЊ103ЁцЃЌвзШмгкЗЧМЋадШмМСЃЌОнДЫПЩХаЖЯE(CO)5ЕФОЇЬхРраЭЮЊ ЁЃ
ЃЈ5ЃЉН№ЪєEЕЅжЪЕФОЇЬхдкВЛЭЌЮТЖШЯТга
СНжжЖбЛ§ЗНЪНЃЌОЇАћЗжБ№ШчЭМЫљЪОЁЃ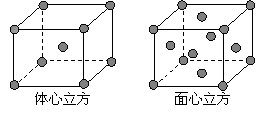 ЬхаФ
ЬхаФ
СЂЗНОЇАћКЭУцаФСЂЗНОЇАћжаЪЕМЪКЌгаЕФE
дзгИіЪ§жЎБШЮЊ____ ___ЁЃ
вбжЊAЁЂBЁЂCЁЂDЁЂEЖМЪЧдЊЫижмЦкБэжаЧАЫФжмЦкЕФдЊЫиЃЌЫќУЧЕФКЫЕчКЩЪ§AЃМBЃМCЃМDЃМEЁЃBдзгЕФpЙьЕРАыГфТњЃЌаЮГЩЕФЧтЛЏЮяЕФЗаЕуЪЧЭЌжїзхдЊЫиЕФЧтЛЏЮяжазюЕЭЕФЁЃDдзгЕУЕНвЛИіЕчзгКѓ3pЙьЕРШЋГфТњЁЃA+БШDдзгаЮГЩЕФРызгЩйвЛИіЕчзгВуЁЃCгыAаЮГЩA2CаЭРызгЛЏКЯЮяЁЃEЕФдзгађЪ§ЮЊ26ЃЌEдзгЛђРызгЭтЮЇгаНЯЖрФмСПЯрНќЕФПеЙьЕРЖјФмгывЛаЉЗжзгЛђРызгаЮГЩХфКЯЮяЁЃ
ЧыИљОнвдЩЯЧщПіЃЌЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉКЌгадЊЫиAЕФбЮЕФбцЩЋЗДгІЮЊ ЁЃаэЖрН№ЪєбЮЖМПЩвдЗЂЩњбцЩЋЗДгІЃЌЦфдвђЪЧ ЁЃ
ЃЈ2ЃЉCЕФЧтЛЏЮяЗжзгЕФМќНЧЪЧ ЃЌЪєгк ЗжзгЁЃЃЈЬюЁАМЋадЁБЛђЁАЗЧМЋадЁБЃЉ
ЃЈ3ЃЉBD3ЕФжааФдзгЕФдгЛЏРраЭЪЧ
ЃЈ4ЃЉEЕФвЛжжГЃМћХфКЯЮяE(CO)5ГЃЮТЯТГЪвКЬЌЃЌШлЕуЮЊ-20.5ЁцЃЌЗаЕуЮЊ103ЁцЃЌвзШмгкЗЧМЋадШмМСЃЌОнДЫПЩХаЖЯE(CO)5ЕФОЇЬхРраЭЮЊ ЁЃ
ЃЈ5ЃЉН№ЪєEЕЅжЪЕФОЇЬхдкВЛЭЌЮТЖШЯТгаСНжжЖбЛ§ЗНЪНЃЌОЇАћЗжБ№ШчЭМЫљЪОЁЃЬхаФСЂЗНОЇАћКЭУцаФСЂЗНОЇАћжаЪЕМЪКЌгаЕФEдзгИіЪ§жЎБШЮЊ____ ___ЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com