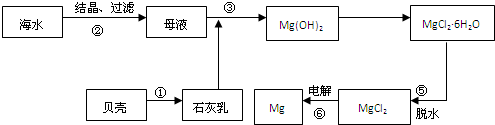
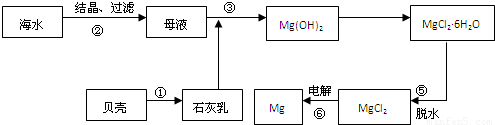
某铝合金中含有镁、铜、硅,为了测定研究它的抗腐蚀性能和测定合金中铝的含量,某研究性学习小组设计了如下实验:
(一)探究铝合金的抗腐蚀性能
①向一只小烧杯里加入20mL0.5mol/LCuSO
4溶液,把一小块铝合金浸入溶液中,1~2分钟后将铝片取出,观察铝片表面的现象
②取1只试管,加入10mL2mol/LNaOH溶液,将一块铝片放入NaOH溶液里,片刻取出后,用蒸馏水冲洗后浸入CuSO
4溶液里.1~2分钟后将铝片取出,观察铝片表面的现象
实验①铝片没有变化,实验②铝片表面的现象是
铝片表面有亮红色的固体附着
铝片表面有亮红色的固体附着
发生此现象的原因是
因为铝片有一层致密的氧化物保护膜,可以阻止内部的金属铝与CuSO4反应,当铝片事先放入氢氧化钠溶液后,这层氧化膜被破坏,金属铝与硫酸铜发生置换反应生成了金属铜.
因为铝片有一层致密的氧化物保护膜,可以阻止内部的金属铝与CuSO4反应,当铝片事先放入氢氧化钠溶液后,这层氧化膜被破坏,金属铝与硫酸铜发生置换反应生成了金属铜.
(二)测定铝合金中的铝的百分含量
①取该样品a克,将样品溶于足量的稀盐酸中,过滤;
②在滤液中加入过量的氢氧化钠溶液,过滤;
③往第②步的滤液中通入足量的CO
2,过滤,将沉淀用蒸馏水洗涤后,烘干并灼烧至质量不再减少为止,冷却后称量,质量为b克.
回答下列问题:
(1)在第①步操作中溶解所使用的玻璃仪器为玻璃棒、
烧杯
烧杯
,滤液中主要含有Mg
2+、Na
+、
Al3+
Al3+
和Cl
-离子;
(2)在第②步操作中氢氧化钠溶液需要过量的原因是
使Al3+全部变成AlO2-离子
使Al3+全部变成AlO2-离子
,写出该步骤中生成沉淀的离子方程式
Mg2++2OH-=Mg(OH)2↓
Mg2++2OH-=Mg(OH)2↓
(3)第③步灼烧过程中可在下列哪种仪器中进行
C
C
A.烧杯 B.试管 C.坩埚 D.蒸发皿
(4)第③步灼烧后得到的固体是
Al2O3
Al2O3
(5)合金中铝的质量分数是
.