
题目列表(包括答案和解析)
 舍勒发现氯气的方法至今还是实验室制取氯气的主要方法之一.
舍勒发现氯气的方法至今还是实验室制取氯气的主要方法之一.(12分)舍勒发现氯气的的方法至今还是实验室制取氯气的主要方法之一.
(1)请写出实验室制氯气的反应化学方程 ,
(2)反应方程式中氧化剂和还原剂物质的量之比为 ;其中Cl2是 产物(填氧化或还原);
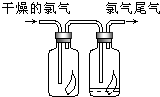
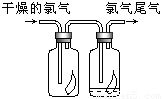
(3)如右图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是 ,从而得出的结论是 .
(4)实验室中剩余的Cl2尾气通常用NaOH溶液吸收,发生反应的离子方程式 。
(12分)舍勒发现氯气的的方法至今还是实验室制取氯气的主要方法之一.
(1)请写出实验室制氯气的反应化学方程 ,
(2)反应方程式中氧化剂和还原剂物质的量之比为 ;其中Cl2是 产物(填氧化或还原);
(3)如右图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是 ,从而得出的结论是 .
(4)实验室中剩余的Cl2尾气通常用NaOH溶液吸收,发生反应的离子方程式 。
舍勒发现氯气的的方法至今还是实验室制取氯气的主要方法之一.
(1)请写出实验室制氯气的反应化学方程 ,
(2)反应方程式中氧化剂和还原剂物质的量之比为 ;其中Cl2是 产物(填氧化或还原);
(3)如右图所示,将氯气依次通过盛有干燥有色布条的广
口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是
,从而得出的结论是 .
(4)实验室中剩余的Cl2尾气通常用NaOH溶液吸收,发生反应的离子方程式 。

1774年,瑞典化学家舍勒发现氯气的同时也发现了氯水对纸张、蔬菜和花具有永久性的漂白作用.1785年法国化学家贝托雷(Claude Louis Berthollet)提出把漂白作用应用于生产,并注意到氯气溶于草木灰水形成的溶液比氯水更浓,漂白能力更强,而且不逸出氯气.1789年英国化学家台耐特(Smithson Tennant)把氯气溶解在石灰乳中,制成了漂白粉.
现在工业上还是采用把氯气通入消石灰或石灰乳的方法制取漂白粉.消石灰要含略少于1%(质量分数)的水,因为极为干燥的消石灰是不跟氯气反应的.生产漂白粉的反应过程比较复杂,主要反应可以表示如下:
2Cl2+3Ca(OH)2![]() Ca(ClO)2+CaCl2·Ca(OH)2·H2O+H2O
Ca(ClO)2+CaCl2·Ca(OH)2·H2O+H2O
在较高级的漂白粉中,氯化可按下面的化学方程式进行,反应比较安全.
2CaCl2·Ca(OH)2·H2O+2Cl2+8H2O![]() Ca(ClO)2+3CaCl2·4H2O
Ca(ClO)2+3CaCl2·4H2O
问题:
(1)漂白粉的成分是什么?漂白粉的有效成分是什么?
(2)用什么标准来衡量漂白粉的质量好坏呢?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com