
ÌâÄ¿Áбí(°üÀ¨´ð°¸ºÍ½âÎö)
| 3 |
| 5 |
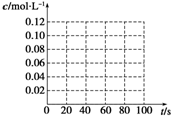 ÔÚ100¡æʱ£¬½«0.40molµÄ¶þÑõ»¯µªÆøÌå³äÈë2LÕæ¿ÕµÄÃܱÕÈÝÆ÷ÖУ¬Ã¿¸ôÒ»¶Îʱ¼ä¾Í¶Ô¸ÃÈÝÆ÷ÄÚµÄÎïÖʽøÐзÖÎö£¬µÃµ½Êý¾ÝÈç±íËùʾ£º
ÔÚ100¡æʱ£¬½«0.40molµÄ¶þÑõ»¯µªÆøÌå³äÈë2LÕæ¿ÕµÄÃܱÕÈÝÆ÷ÖУ¬Ã¿¸ôÒ»¶Îʱ¼ä¾Í¶Ô¸ÃÈÝÆ÷ÄÚµÄÎïÖʽøÐзÖÎö£¬µÃµ½Êý¾ÝÈç±íËùʾ£º| ʱ¼ä£¨s£© | 0 | 20 | 40 | 60 | 80 |
| n£¨NO2£©/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n£¨N2O4£©/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
¹ú¼ÊѧУÓÅÑ¡ - Á·Ï°²áÁбí - ÊÔÌâÁбí
ºþ±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨Æ½Ì¨ | ÍøÉÏÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | µçÐÅթƾٱ¨×¨Çø | ÉæÀúÊ·ÐéÎÞÖ÷ÒåÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com