
题目列表(包括答案和解析)
(14分)下表为一元素周期表(空白,未填元素)根据要求填空。
| ① |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| ② | ③ | ④ |
|
|
| ⑤ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| 丙 |
|
| 丁 |
| 甲 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| 乙 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
⑴ 在上面元素周期表中,全部是金属元素的区域为 (填字母代号)
A.甲 B.乙 C.丙 D.丁
⑵用实线画出金属与非金属的分界线(在答题卷图上完成)。
⑶已知R元素的某种原子的质量数为31,且原子核内质子数比中子数少1,请在答题卷中的周期表中标出“R” 元素的位置(在答题卷图上完成)。
⑷在我们常用的周期表中,①元素的位置比较尴尬,它是第1列的唯一非金属元素。有人认为也可把①元素放在VIIA族,支持这个观点的物质是___ _______。
A.HF B.H+ C.NaH D.H2O2
⑸由①②③④四种元素形成的原子个数比为5:1:1:3一种离子化合物的化学式为__ ____;该化合物与过量⑤的氧化物的水化物微热时反应的离子方程式是 ;
若用球棍模型表示①和④形成的化合物的分子结构,应该是 。
(14分)下表为一元素周期表(空白,未填元素)根据要求填空。
| ① | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | ② | ③ | ④ | | |
| ⑤ | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | 丙 | | | 丁 |
| 甲 | | | | | | | | | | | | | | | | | |
| | | | | | | 乙 | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | |

[2012·天津卷](14分)信息时代产生的大量电子垃圾对环境构成了极大的威胁。某“变废为宝”学生探究小组将一批废弃的线路板简单处理后,得到含70%Cu、25%Al、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线: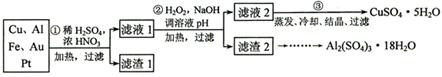
请回答下列问题:
(1)第①步Cu与酸反应的离子方程式为_______________________________;得到滤渣1的主要成分为___________________。
(2)第②步加H2O2的作用是________________,使用H2O2的优点是
;调溶液pH的目的是使 生成沉淀。
(3)用第③步所得CuSO4·5H2O制备无水CuSO4的方法是 。
(4)由滤渣2制取Al2(SO4)3·18H2O ,探究小组设计了三种方案:
上述三种方案中,_______方案不可行,原因是_____________________________;从原子利用率角度考虑,________方案更合理。
(5)探究小组用滴定法测定CuSO4·5H2O (Mr=250)含量。取a g试样配成100 mL溶液,每次取20.00 mL,消除干扰离子后,用cmol·L-1 EDTA(H2Y2-)标准溶液滴定至终点,平均消耗EDTA溶液bmL。滴定反应如下:
Cu2++H2Y2-=CuY2-+2H+
写出计算CuSO4·5H2O质量分数的表达式w= ________________ ;下列操作会导致CuSO4·5H2O含量的测定结果偏高的是_____________。
a.未干燥锥形瓶
b.滴定终点时滴定管尖嘴中产生气泡
c.未除净可与EDTA反应的干扰离子
[2012·天津卷](14分)信息时代产生的大量电子垃圾对环境构成了极大的威胁。某“变废为宝”学生探究小组将一批废弃的线路板简单处理后,得到含70%Cu、25%Al、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:
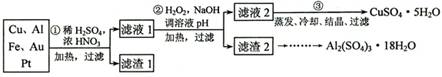
请回答下列问题:
(1)第①步Cu与酸反应的离子方程式为_______________________________;得到滤渣1的主要成分为___________________。
(2)第②步加H2O2的作用是________________,使用H2O2的优点是
;调溶液pH的目的是使 生成沉淀。
(3)用第③步所得CuSO4·5H2O制备无水CuSO4的方法是 。
(4)由滤渣2制取Al2(SO4)3·18H2O ,探究小组设计了三种方案:
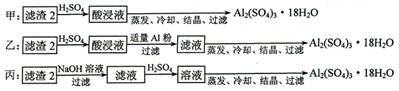
上述三种方案中,_______方案不可行,原因是_____________________________;从原子利用率角度考虑,________方案更合理。
(5)探究小组用滴定法测定CuSO4·5H2O (Mr=250)含量。取a g试样配成100 mL溶液,每次取20.00 mL,消除干扰离子后,用c mol·L-1 EDTA(H2Y2-)标准溶液滴定至终点,平均消耗EDTA溶液bmL。滴定反应如下:
Cu2++H2Y2-=CuY2-+2H+
写出计算CuSO4·5H2O质量分数的表达式w= ________________ ;下列操作会导致CuSO4·5H2O含量的测定结果偏高的是_____________。
a.未干燥锥形瓶
b.滴定终点时滴定管尖嘴中产生气泡
c.未除净可与EDTA反应的干扰离子
(14分)下表为一元素周期表(空白,未填元素)根据要求填空。
|
① |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
② |
③ |
④ |
|
|
|
⑤ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
丙 |
|
|
丁 |
|
甲 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
乙 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
⑴ 在上面元素周期表中,全部是金属元素的区域为 (填字母代号)
A.甲 B.乙 C.丙 D.丁
⑵用实线画出金属与非金属的分界线(在答题卷图上完成)。
⑶已知R元素的某种原子的质量数为31,且原子核内质子数比中子数少1,请在答题卷中的周期表中标出“R” 元素的位置(在答题卷图上完成)。
⑷在我们常用的周期表中,①元素的位置比较尴尬,它是第1列的唯一非金属元素。有人认为也可把①元素放在VIIA族,支持这个观点的物质是___ _______。
A.HF B.H+ C.NaH D.H2O2
⑸由①②③④四种元素形成的原子个数比为5:1:1:3一种离子化合物的化学式为__ ____;该化合物与过量⑤的氧化物的水化物微热时反应的离子方程式是 ;
若用球棍模型表示①和④形成的化合物的分子结构,应该是 。

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com