
题目列表(包括答案和解析)
| 名称 | 化学式 | 颜色、状态 | 溶解度(g) | 熔点(℃) | 密度(g/cm3) |
| 乙二酸 | H2C2O4 | ― | 8.6(20℃) | 189.5 | 1.900 |
| 二水合乙二酸 | H2C22?2H2O | 无色晶体 | ― | 101.5 | 1.650 |
注:乙二酸(HOOC―COOH)俗称草酸,带2个结晶水的乙二酸俗称草酸晶体,草酸晶体失去结晶水得无水草酸,在约157℃时升华,其盐草酸钙和草酸氢钙均为白色不溶物。
根据上述信息,回答下列问题。
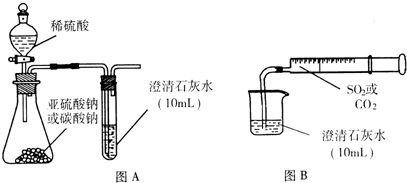
(1)向盛有Na2CO3粉末的试管里加入约3mL乙二酸溶液,观察到的现象是 ,说明乙二酸的酸性比碳酸 (填“强”或“弱”)。
(2)向盛有5mL乙二酸饱和溶液的试管中滴入3滴用硫酸酸化的0.5%(质量分数)的高锰酸钾溶液,振荡,观察到的现象为 _______ ,说明乙二酸有_____ 性。
(3)向A试管中加入3mL乙二酸,然后边振荡试管边加入2mL浓硫酸和2mL乙二酸,按下图甲连接好装置,加热3 -5min,在B管中有油状且带有香味的液体产生,该现象说明发生了 反应(填有机反应类型)。在B试管中加入饱和 Na2CO3溶液的目的是 。
B中导管口在液面上的原因是 。
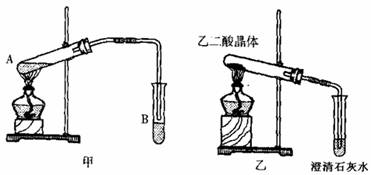
(4)已知草酸分解的化学方程式为:H2C2O4 ![]() H2O+CO2↑+CO↑,用图乙装置加热草酸晶体,验证草酸受热分解及其产物,但有人认为该装置不合理。请你根据相关信息的实验目的,分析不合理原因 (从下列序号中选择)。
H2O+CO2↑+CO↑,用图乙装置加热草酸晶体,验证草酸受热分解及其产物,但有人认为该装置不合理。请你根据相关信息的实验目的,分析不合理原因 (从下列序号中选择)。
a.草酸晶体的熔点较低,未分解之前就已融化并流到试管口,不利于化学反应的进行及实验现象的观察。
b.因为加热是草酸晶体,所以该装置最多只能检验一种分解产物,不能检验是否
还有其他分解产物。
c.在未洗气的情况下通入石灰水,还可能因草酸蒸汽与石灰水反应生成草酸钙沉淀,对实验有干扰。
(5)该装置也不附合绿色化学的要求试说明原因 。

利用15N可以测定亚硝酸盐对地下水质的污染情况。
(1)下列说法正确的是___。
A.14N与15N为同种核素
B. 14N的第一电离能小于14C
C. 15NH3与14NH3均能形成分子间氢键
D. CH315NH2与CH3CH214NH2互为同系物
(2)15N的价层电子排布图为_______15NH4Cl的晶胞与CsCl相同,则15NH4Cl晶体中15NH4+的配位数为_______;15NH4+中I5N的杂化轨道类型为_______。
(3) 工业上电解法处理亚硝酸盐的模拟工艺如图。
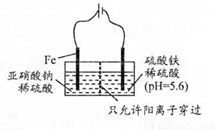
已知:阳极区发生化学反应:
2NO2-+8H++6Fe2+==N2↑ +6Fe3++4HzO
①阳极电极反应方程式是______(不考虑后续反应);
②若硫酸溶液浓度过大,阴极区会有气体逸出,该气体为______(填化学式);该现象表明c( H+ )越大,H+氧化性越______;
③若电解时电路中有0.6 mol电子转移,且NaNO2有剩余,则电解池中生成Na2SO4 ______mol。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com