
ÌâÄ¿Áбí(°üÀ¨´ð°¸ºÍ½âÎö)
(12·Ö)»¯Ñ§·´Ó¦¹ý³ÌÖз¢ÉúÎïÖʱ仯µÄͬʱ£¬³£³£°éÓÐÄÜÁ¿µÄ±ä»¯£¬ÕâÖÖÄÜÁ¿µÄ±ä»¯³£ÒÔÈÈÄܵÄÐÎʽ±íÏÖ³öÀ´£¬½Ð×ö·´Ó¦ÈÈ¡£ÓÉÓÚ·´Ó¦µÄÇé¿ö²»Í¬£¬·´Ó¦ÈÈ¿ÉÒÔ·ÖΪÐí¶àÖÖ£¬ÈçȼÉÕÈȺÍÖкÍÈȵȡ£
£¨1£©ÏÂÁЦ¤H±íʾÎïÖÊȼÉÕÈȵÄÊÇ £»±íʾÎïÖÊÖкÍÈȵÄÊÇ ¡£
(Ìî¡°¦¤H1¡±¡¢¡°¦¤H2¡±ºÍ¡°¦¤H3¡±µÈ)
A£®2H2(g)+O2(g) = 2H2O(l) ¡¡¦¤H1
B£®C(s)+1/2O2(g) = CO(g)¡¡¦¤H2
C£®CH4(g)+2O2(g) = CO2(g)+2H2O(g)¡¡¦¤H3
D£®C(s)+O2(g)= CO2(g) ¡¡¦¤H4
E£®C6H12O6(s)+6O2(g) = 6CO2(g)+6H2O(l)¡¡¦¤H5
F£®NaOH(aq)+HCl(aq) = NaCl(aq)+H2O(l)¡¡¦¤H6
G£®2NaOH(aq)+H2SO4(aq) = Na2SO4(aq)+2H2O(l) ¦¤H7
£¨2£©ÒÑÖªÔÚ101kPa¡¢273Kʱ£¬15gÒÒÍéȼÉÕÉú³ÉCO2ºÍҺ̬ˮ£¬·Å³öakJµÄÈÈÁ¿£¬ÏÂÁÐÈÈ»¯Ñ§·½³ÌʽÕýÈ·µÄÊÇ ¡£
A£®C2H6(g)+7/2O2(g) = 2CO2(g)+3H2O(l) ¦¤H= +2akJ/mol
B£®C2H6(g)+7/2O2(g) = 2CO2(g)+3H2O(g) ¦¤H= -2akJ/mol
C£®2C2H6(g)+7O2(g) = 4CO2(g)+6H2O(l) ¦¤H= -4akJ/mol
D£®2C2H6(g)+7O2(g) = 4CO2(g)+6H2O(g) ¦¤H= -4akJ/mol
£¨3£©½øÒ»²½Ñо¿±íÃ÷£¬»¯Ñ§·´Ó¦µÄÄÜÁ¿±ä»¯(¦¤H)Óë·´Ó¦ÎïºÍÉú³ÉÎïµÄ¼üÄÜÓйأ¨¼üÄÜ¿ÉÒÔ¼òµ¥µØÀí½âΪ¶Ï¿ª1mol»¯Ñ§¼üʱËùÐèÎüÊÕµÄÄÜÁ¿£©£¬Ï±íÊDz¿·Ö»¯Ñ§¼üµÄ¼üÄÜÊý¾Ý£º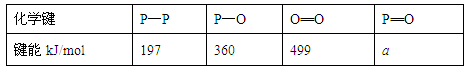
ÒÑÖª°×Á×(P4)µÄȼÉÕÈÈΪ2378.0kJ/mol£¬°×Á×ÍêȫȼÉյIJúÎï(P4O10)µÄ½á¹¹ÈçÏÂͼËùʾ£¬ÔòÉϱíÖÐa= ¡£
£¨4£©ÔÚ25¡æ¡¢101kPaÏ£¬1g¼×´¼È¼ÉÕÉú³ÉCO2ºÍҺ̬ˮʱ·ÅÈÈ22.68kJ¡£Ôò±íʾ¼×´¼È¼ÉÕÈȵÄÈÈ»¯Ñ§·½³ÌʽΪ ¡£
ÒÑÖª·´Ó¦£º¢ÙAl+Fe2O3 Al2O3+Fe ¡÷H£½a kJ/mol
Al2O3+Fe ¡÷H£½a kJ/mol
¢Ú101kPaʱ£¬2C(s)£«O2(g)£½2CO£¨g£©¡÷H£½£221 kJ/mol
¢ÛÏ¡ÈÜÒºÖУ¬H£«(aq)£«OH£(aq)£½H2O(1)¡÷H£½£57.3 kJ/mol
¢ÜºìÁ׵Ļ¯Ñ§Ê½ÎªP£¬°×Á׵Ļ¯Ñ§Ê½ÎªP4£¬ÒÑÖª£ºP4(s)+5O2(g)=P4O10(s) ¡÷H£½£3093.2 kJ/mol 4P (s)+5O2(g)=P4O10(s) ¡÷H£½£2954.0 kJ/mol ÏÂÁнáÂÛÕýÈ·µÄÊÇ
A£®ÂÁÈÈ·´Ó¦ÔÚ¸ßÎÂϲÅÄÜ·¢Éú£¬Òò´Ëa>0
B£®Ì¼µÄȼÉÕÈȵÈÓÚ110.5 kJ/mol
C£®Ï¡´×ËáÓëÏ¡NaOHÈÜÒº·´Ó¦Éú³É1 molË®£¬·Å³öÈÈÁ¿Ð¡ÓÚ57.3 kJ
D£®ÓÉÌõ¼þ¿ÉÖª£ººìÁ×ת»¯Îª°×Á×ÊÇ·ÅÈÈ·´Ó¦£¬ËùÒÔµÈÖÊÁ¿µÄºìÁ×ÄÜÁ¿±È°×Á×µÍ
£¨1£©ÒÑÖª£ºP4£¨°×Á×£¬s£©£«5O2£¨g£©£½P4O10£¨s£© ¦¤H£½£2983.2kJ/mol
P£¨ºìÁ×£¬s£©£«5/4O2£¨g£©£½1/4 P4O10£¨s£© ¦¤H£½£738.5kJ/mol
Ôò°×Á×ת»¯ÎªºìÁ×µÄÈÈ»¯Ñ§·½³ÌʽΪ £»ÓÉ´Ë˵Ã÷ºìÁ×µÄÎȶ¨ÐԱȰ×Á× ¡£
£¨2£©Ã÷·¯[KAl(SO4)2¡¤12H2O]Ë®ÈÜÒº³Ê £¨Ìî¡°Ëᡱ¡¢¡°¼î¡±»ò¡°ÖС±£©ÐÔ£»Ã÷·¯»¹Äܾ»Ë®£¬ÓÃÀë×Ó·½³Ìʽ½âÊÍÆäÔÒòΪ ¡£
£¨3£©µç½â³ØµÄÄÜÁ¿×ª»¯ÐÎʽΪ £¬Ôµç³Ø·´Ó¦ £¨Ìî¡°Ò»¶¨¡±»ò¡°²»Ò»¶¨¡±£©×Ô·¢¡£
£¨4£©pH=3µÄÑÎËáºÍpH=3µÄ´×ËáÈÜÒº¸÷Ï¡ÊÍÖÁÆäÌå»ýµÄ100±¶£¬Ï¡ÊͺóÑÎËáµÄpH (Ìî¡°´óÓÚ¡±¡¢¡°Ð¡ÓÚ¡±»ò¡°µÈÓÚ¡±)´×ËáµÄpH£»³£ÎÂʱpH=xµÄÑÎËáºÍpH=yµÄNaOHÈÜÒºÒÔ1©U10µÄÌå»ý±È»ìºÏ£¬·´Ó¦ºóÈÜҺǡºÃ³ÊÖÐÐÔ£¬Ôòx¡¢yÂú×ãµÄ¹ØϵÊÇ ¡£
(12·Ö)(2011¡¤Òø´¨¸ß¶þ¼ì²â)»¯Ñ§·´Ó¦¹ý³ÌÖз¢ÉúÎïÖʱ仯µÄͬʱ£¬³£³£°éÓÐÄÜÁ¿µÄ±ä»¯£¬ÕâÖÖÄÜÁ¿µÄ±ä»¯³£ÒÔÈÈÄܵÄÐÎʽ±íÏÖ³öÀ´£¬½Ð×ö·´Ó¦ÈÈ¡£ÓÉÓÚ·´Ó¦µÄÇé¿ö²»Í¬£¬·´Ó¦ÈÈ¿ÉÒÔ·ÖΪÐí¶àÖÖ£¬ÈçȼÉÕÈȺÍÖкÍÈȵȡ£
(1)ÏÂÁЦ¤H±íʾÎïÖÊȼÉÕÈȵÄÊÇ________£»±íʾÎïÖÊÖкÍÈȵÄÊÇ________¡£(ÌH1¡¢¦¤H2ºÍ¦¤H3µÈ)
| A£®2H2(g)£«O2(g)===2H2O(l)¡¡¦¤H1 |
| B£®C(s)£«O2(g)===CO(g)¡¡¦¤H2 |
| C£®CH4(g)£«2O2(g)===CO2(g)£«2H2O(g)¡¡¦¤H3 |
| D£®C(s)£«O2(g)===CO2(g)¡¡¦¤H4 |
| »¯Ñ§¼ü | P¡ªP | P¡ªO | O===O | P===O |
| ¼üÄÜkJ/mol | 197 | 360 | 499 | x |

(12·Ö)»¯Ñ§·´Ó¦¹ý³ÌÖз¢ÉúÎïÖʱ仯µÄͬʱ£¬³£³£°éÓÐÄÜÁ¿µÄ±ä»¯£¬ÕâÖÖÄÜÁ¿µÄ±ä»¯³£ÒÔÈÈÄܵÄÐÎʽ±íÏÖ³öÀ´£¬½Ð×ö·´Ó¦ÈÈ¡£ÓÉÓÚ·´Ó¦µÄÇé¿ö²»Í¬£¬·´Ó¦ÈÈ¿ÉÒÔ·ÖΪÐí¶àÖÖ£¬ÈçȼÉÕÈȺÍÖкÍÈȵȡ£
£¨1£©ÏÂÁЦ¤H±íʾÎïÖÊȼÉÕÈȵÄÊÇ £»±íʾÎïÖÊÖкÍÈȵÄÊÇ ¡£
(Ìî¡°¦¤H1¡±¡¢¡°¦¤H2¡±ºÍ¡°¦¤H3¡±µÈ)
A£®2H2(g)+O2(g) = 2H2O(l) ¡¡¦¤H1
B£®C(s)+1/2O2(g) = CO(g)¡¡¦¤H2
C£®CH4(g)+2O2(g) = CO2(g)+2H2O(g)¡¡¦¤H3
D£®C(s)+O2(g)= CO2(g) ¡¡¦¤H4
E£®C6H12O6(s)+6O2(g) = 6CO2(g)+6H2O(l)¡¡¦¤H5
F£®NaOH(aq)+HCl(aq) = NaCl(aq)+H2O(l)¡¡¦¤H6
G£®2NaOH(aq)+H2SO4(aq) = Na2SO4(aq)+2H2O(l) ¦¤H7
£¨2£©ÒÑÖªÔÚ101kPa¡¢273Kʱ£¬15gÒÒÍéȼÉÕÉú³ÉCO2ºÍҺ̬ˮ£¬·Å³öakJµÄÈÈÁ¿£¬ÏÂÁÐÈÈ»¯Ñ§·½³ÌʽÕýÈ·µÄÊÇ ¡£
A£®C2H6(g)+7/2O2(g) = 2CO2(g)+3H2O(l) ¦¤H= +2akJ/mol
B£®C2H6(g)+7/2O2(g) = 2CO2(g)+3H2O(g) ¦¤H= -2akJ/mol
C£®2C2H6(g)+7O2(g) = 4CO2(g)+6H2O(l) ¦¤H= -4akJ/mol
D£®2C2H6(g)+7O2(g) = 4CO2(g)+6H2O(g) ¦¤H= -4akJ/mol
£¨3£©½øÒ»²½Ñо¿±íÃ÷£¬»¯Ñ§·´Ó¦µÄÄÜÁ¿±ä»¯(¦¤H)Óë·´Ó¦ÎïºÍÉú³ÉÎïµÄ¼üÄÜÓйأ¨¼üÄÜ¿ÉÒÔ¼òµ¥µØÀí½âΪ¶Ï¿ª1mol»¯Ñ§¼üʱËùÐèÎüÊÕµÄÄÜÁ¿£©£¬Ï±íÊDz¿·Ö»¯Ñ§¼üµÄ¼üÄÜÊý¾Ý£º

ÒÑÖª°×Á×(P4)µÄȼÉÕÈÈΪ2378.0kJ/mol£¬°×Á×ÍêȫȼÉյIJúÎï(P4O10)µÄ½á¹¹ÈçÏÂͼËùʾ£¬ÔòÉϱíÖÐa= ¡£

£¨4£©ÔÚ25¡æ¡¢101kPaÏ£¬1g¼×´¼È¼ÉÕÉú³ÉCO2ºÍҺ̬ˮʱ·ÅÈÈ22.68kJ¡£Ôò±íʾ¼×´¼È¼ÉÕÈȵÄÈÈ»¯Ñ§·½³ÌʽΪ ¡£
¹ú¼ÊѧУÓÅÑ¡ - Á·Ï°²áÁбí - ÊÔÌâÁбí
ºþ±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨Æ½Ì¨ | ÍøÉÏÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | µçÐÅթƾٱ¨×¨Çø | ÉæÀúÊ·ÐéÎÞÖ÷ÒåÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com