(2008?闵行区模拟)在高中阶段,我们学习了两种酯的实验室制备方法:
①乙酸乙酯的制备(装置如图1);
②乙酸丁酯[CH
3COO(CH
2)
3CH
3]的制备(装置如图2).

制备这两种酯所涉及的有关物质的物理性质见表:
| 物理性质 |
乙酸 |
乙醇 |
1-丁醇 |
乙酸乙酯 |
乙酸丁酯 |
| 熔点(℃) |
16.6 |
-117.3 |
-89.5 |
-83.6 |
-73.5 |
| 沸点(℃) |
117.9 |
78.5 |
117 |
77.06 |
126.3 |
| 密度(g/cm3) |
1.05 |
0.79 |
0.81 |
0.90 |
0.88 |
请回答下列问题:
(1)在乙酸乙酯的制备过程中,采用水浴加热的优点为
受热均匀,易控制温度
受热均匀,易控制温度
;制备乙酸丁酯的过程中,直玻璃管的作用是
冷凝回流
冷凝回流
,试管不与石棉网直接接触的原因是
防止加热温度过高,有机物碳化分解.
防止加热温度过高,有机物碳化分解.
.
(2)乙酸乙酯制备时,饱和Na
2CO
3溶液的作用是
除去乙酸乙酯中的乙酸和乙醇,降低乙酸乙酯的溶解度,便于分层
除去乙酸乙酯中的乙酸和乙醇,降低乙酸乙酯的溶解度,便于分层
.两种酯的提纯过程中都需用到的关键仪器是
分液漏斗
分液漏斗
,在操作时要充分振荡、静置,待液体分层后先将水溶液放出,最后将所制得的酯从该仪器的
A
A
(填序号).
A.上口倒出 B.下部流出 C.都可以
(3)在乙酸丁酯制备中,下列方法可提高1-丁醇的利用率的是
B、C
B、C
(填序号).
A.使用催化剂 B.加过量乙酸 C.不断移去产物 D.缩短反应时间
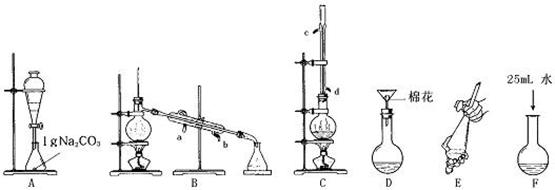
(4)1-丁醇若含有乙醇,有同学认为制得的乙酸丁酯中含有乙酸乙酯.为了证实该观点,可尝试选用下列
C
C
(填序号)装置来做实验,请简述与实验结论有关的实验过程和现象
将制得的乙酸丁酯进行蒸馏,看能否得到78℃左右的馏分,且该馏分不溶于饱和碳酸钠溶液
将制得的乙酸丁酯进行蒸馏,看能否得到78℃左右的馏分,且该馏分不溶于饱和碳酸钠溶液
.


 (2012?闸北区二模)苯甲酸甲酯是一种重要的工业原料,某化学小组采用如图装置,以苯甲酸、甲醇为原料制取苯甲酸甲酯.有关物质的物理性质见下表所示:
(2012?闸北区二模)苯甲酸甲酯是一种重要的工业原料,某化学小组采用如图装置,以苯甲酸、甲醇为原料制取苯甲酸甲酯.有关物质的物理性质见下表所示:
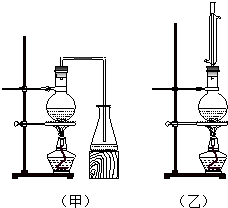 实验室制取乙酸丁酯的实验装置有如图甲、乙两种装置可供选用.
实验室制取乙酸丁酯的实验装置有如图甲、乙两种装置可供选用.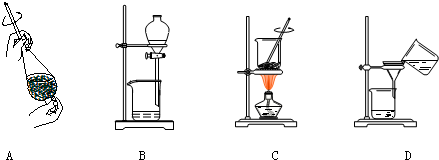


 G H I
G H I