
题目列表(包括答案和解析)

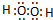
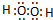

| ||
| ||
 则:
则:


| ||
| ||
已知:①标准状况下,1体积水中最多能溶解500体积的HCl;
②饱和NaCl溶液的浓度约为5.00 mol·L-1。
在标准状况下,将448 L HCl气体溶于1 L水中,所得溶液A的密度为1.20 g·cm-3,则溶液A中HCl的物质的量浓度为 。(本题计算结果均取三位有效数字)
(1)若使Cl-浓度与溶液A中的Cl-浓度相等,则在1 L NaCl饱和溶液中还应溶解约 L标准状况下HCl气体 (溶液体积变化忽略不计)。
(2)取10.0 mL溶液A稀释成500 mL溶液B,则溶液B中HCl的物质的量浓度为 。
(3)在溶液B的配制过程中,使用前必须检查是否漏液的仪器有 ;下列配制操作,造成溶液B浓度偏低的是_______________(选填序号)。
a.容量瓶用蒸馏水洗涤后未干燥
b.量取溶液A的量筒用蒸馏水洗涤后未干燥
c.定容时,俯视液面加水至刻度线
d.加水定容时液面不慎超过刻度线,立即用胶头滴管吸出部分水使液面刚好达刻度线
e.烧杯中溶液移入容量瓶后,未用水洗涤烧杯和玻璃棒即定容

请回答:
(1)A的化学式为____________;B分子的电子式为____________。
(2)已知E与含A中某种元素的酸在一定条件下反应,产生一种含有该元素的气体X。某校化学兴趣小组为研究该气体的性质,设计下图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。

①装入药品前,检查Ⅰ中气体发生装置气密性的操作是______________________________;
②写出装置Ⅰ中发生反应的离子方程式____________________________________________;
③实验过程中,观察到装置Ⅳ中出现淡黄色沉淀,其主要反应的离子方程式为__________;
④实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为在装置(选填装置序号)___________之间,还需添加洗气瓶,该装置的作用是________________________________________________;
(3)气体X能与溶液B反应,生成气体D,写出反应的化学方程式:________________。
已知A、B、D、E四种物质中均含有同一种短周期元素,D为气体单质,E为黑色粉末,它们有如图所示转化关系(某些产物已略去)。
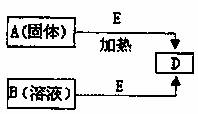
请回答:
(1)A的化学式为 ;B分子的电子式为 。
(2)已知E与含A中某元素的酸在一定条件下反应,产生一种含该元素的气体X。某化学兴趣小组为研究该气体的性质,设计如图所示装置进行试验。装置III中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
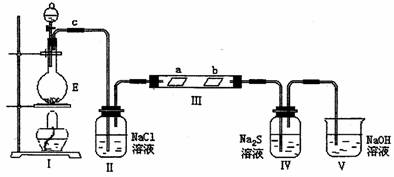
①加入式试剂前,检验气体发生装置I的气密性的操作是:
②写出装置I中发生反应的离子方程式:
③实验过程中,观察到装置IV中出现淡黄色沉淀,其主要反应的离子方程式为:
④实验结束后,该小组同学观察到在装置III中的b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为达到这一预期目的,你认为应对实验装置作如何改进
(3)气体X能与溶液B反应,生成气体D,写出该变化的化学方程式:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com