
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)



A°¢B°¢C°¢D°¢EŒ™«∞Àƒ÷Ð∆⁄÷–‘≠◊”–Ú ˝“¿¥Œ‘ˆ¥Ûµƒ‘™Àÿ£¨œýπÿµƒ–≈œ¢»Áœ¬£∫
‘™Àÿ œýπÿ–≈œ¢
A A‘™Àÿ‘≠◊”∫ÀÕ‚÷ª”–»˝∏ˆƒÐº∂£¨«“√ø∏ˆƒÐº∂…œ∫¨”–œýµ»µƒµÁ◊” ˝
B «ø’∆¯÷–∫¨¡ø◊Ó∑·∏ªµƒ‘™Àÿ
C ∂Ã÷Ð∆⁄÷–£¨µ•÷ CµƒΩ Ù–‘◊Ó«ø
D ª˘Ã¨‘≠◊”µ⁄»˝ƒÐ≤„…œ”–7÷÷‘À∂Ø◊¥Ã¨≤ªÕ¨µƒµÁ◊”
E “ª÷÷∫ÀÀÿµƒ÷ ¡ø ˝Œ™63£¨÷–◊” ˝Œ™34
«Î”√∂‘”¶µƒ‘™Àÿ∑˚∫≈ªÿ¥œ¬¡–Œ £∫
£®1£©A”Ϋ‚ø…–Œ≥…“ª÷÷µƒ∑÷◊” ΩŒ™A2H4ªØ∫œŒÔ£¨∏√∑÷◊”÷–¥Ê‘⁄¶“º¸”ζ–º¸ ˝ƒø±»Œ™ °£
£®2£©H°™A°¢H°™B¡Ω÷÷π≤º€º¸÷–£¨º¸ƒÐΩœ¥Ûµƒ « £ªH°™A°¢H°™D¡Ω÷÷π≤º€º¸÷–£¨º¸µƒº´–‘Ωœ«øµƒ «
£®3£©EŒª”⁄÷Ð∆⁄±Ì÷–µƒŒª÷√ « £¨µ•÷ E”ÎBµƒ◊Ó∏þº€—ıªØŒÔµƒÀƪ،Եƒœ°»Ð“∫∑¥”¶µƒ¿Î◊”∑Ω≥Ã ΩŒ™ °£
£®4£©∏˘æ𜬡–ƒÐ¡ø±‰ªØ æ“‚Õº£¨«Î–¥≥ˆBO∫ÕAO2 ∑¥”¶µƒ»»ªØ—ß∑Ω≥Ã Ω °£

£®5£©Cµƒ◊Ó∏þº€—ıªØŒÔ∂‘”¶µƒÀƪ،Ԍ™M£¨M÷–∫¨”–µƒªØ—ߺ¸¿ý–ÕŒ™ °£Ω´“ª∂®¡øµƒD2 Õ®»Î“ª∂®≈®∂»MµƒÀƻГ∫÷–£¨¡Ω’þ«°∫√ÕÍ»´∑¥”¶ ±£¨…˙≥…ŒÔ÷–”–»˝÷÷∫¨D‘™Àÿµƒ¿Î◊”£¨∆‰÷–¡Ω÷÷¿Î◊”µƒŒÔ÷ µƒ¡ø£®n£©”Î∑¥”¶ ±º‰£®t£©µƒ±‰ªØ æ“‚Õº»Á…œÕºÀ˘ æ°£«Î–¥≥ˆt2 ±øÃ◊Ð∑¥”¶∑Ω≥à Ω
”–a°¢b°¢cÀƒ÷÷Ω Ù£¨Ω´a”Îb”√µºœþ¡¨Ω·∆¿¥Ω˛»ÎµÁΩ‚÷ »Ð“∫÷–£¨b≤ª“◊∏Ø ¥£ÆΩ´a°¢c∑÷±Õ∂»Îµ»≈®∂»µƒ—ŒÀ·÷–£¨c±»a∑¥”¶æÁ¡“£Ææð¥À≈–∂œÀ¸√«µƒªÓ∂Ø–‘”…«øµΩ»ıµƒÀ≥–Ú «( )
A£Æc°¢a°¢b B£Æa°¢b°¢c C£Æb°¢a°¢c D£Æb°¢a°¢c
A°¢B°¢C°¢DÀƒ÷÷∂Ã÷Ð∆⁄‘™Àÿ£¨A‘™Àÿ”–»˝∏ˆµÁ◊”≤„£¨∆‰÷–◊ÓÕ‚≤„µÁ◊” ˝’º◊еÁ◊” ˝µƒ1/6£ªB‘™Àÿ‘≠◊”∫ÀÕ‚µÁ◊” ˝±»A‘™Àÿ‘≠◊”∫ÀÕ‚µÁ◊” ˝∂ý1£ªC£≠¿Î◊”∫ÀÕ‚µÁ◊”≤„ ˝±»A‘™Àÿµƒ¿Î◊”∫ÀÕ‚µÁ◊”≤„ ˝∂ý1£ªD‘™Àÿ‘≠◊”◊ÓÕ‚≤„µÁ◊” ˝ «¥ŒÕ‚≤„µƒ2±∂°£«ÎÃÓ–¥œ¬¡–ø’∏Ò£∫
£®1£©«Î–¥≥ˆAµƒ‘™Àÿ∑˚∫≈ £ª
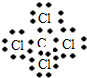
£®2£©Cµƒ“ªº€“ı¿Î◊”µƒΩ·ππ æ“‚Õº £ª
Bµƒ‘≠◊”µƒΩ·ππ æ“‚Õº £ª
£®3£©A°¢B¡Ω‘™Àÿœý±»Ωœ£¨A‘™ÀÿµƒΩ Ù–‘Ωœ«ø£¨ø…“‘—È÷§∏√Ω·¬€µƒ µ—È «£® £©°£
A£ÆΩ´’‚¡Ω÷÷‘™ÀÿµƒøÈ◊¥µ•÷ ∑÷±∑≈»Î¿‰ÀÆ÷–
B£ÆΩ´’‚¡Ω÷÷‘™Àÿµƒµ•÷ ∑÷±∫ÕÕ¨≈®∂»µƒ—ŒÀ·∑¥”¶
C£ÆΩ´’‚¡Ω÷÷‘™Àÿµƒµ•÷ ∑€ƒ©∑÷±∫Õ»»ÀÆ◊˜”√£¨≤¢µŒ»Î∑”Ù ‘“∫
D£Æ±»Ωœ’‚¡Ω÷÷‘™Àÿµƒ∆¯Ã¨«‚ªØŒÔµƒ»»Œ»∂®–‘
A°¢B°¢C°¢DÀƒ÷÷∂Ã÷Ð∆⁄‘™Àÿ£¨A‘™Àÿ”–»˝∏ˆµÁ◊”≤„£¨∆‰÷–◊ÓÕ‚≤„µÁ◊” ˝’º◊еÁ◊” ˝µƒ1/6£ªB‘™Àÿ‘≠◊”∫ÀÕ‚µÁ◊” ˝±»A‘™Àÿ‘≠◊”∫ÀÕ‚µÁ◊” ˝∂ý1£ªC£≠¿Î◊”∫ÀÕ‚µÁ◊”≤„ ˝±»A‘™Àÿµƒ¿Î◊”∫ÀÕ‚µÁ◊”≤„ ˝∂ý1£ªD‘™Àÿ‘≠◊”◊ÓÕ‚≤„µÁ◊” ˝ «¥ŒÕ‚≤„µƒ2±∂°£«ÎÃÓ–¥œ¬¡–ø’∏Ò£∫
£®1£©«Î–¥≥ˆAµƒ‘™Àÿ∑˚∫≈ £ª
£®2£©Cµƒ“ªº€“ı¿Î◊”µƒΩ·ππ æ“‚Õº £ª
Bµƒ‘≠◊”µƒΩ·ππ æ“‚Õº £ª
£®3£©A°¢B¡Ω‘™Àÿœý±»Ωœ£¨A‘™ÀÿµƒΩ Ù–‘Ωœ«ø£¨ø…“‘—È÷§∏√Ω·¬€µƒ µ—È «£® £©°£
A£ÆΩ´’‚¡Ω÷÷‘™ÀÿµƒøÈ◊¥µ•÷ ∑÷±∑≈»Î¿‰ÀÆ÷–
B£ÆΩ´’‚¡Ω÷÷‘™Àÿµƒµ•÷ ∑÷±∫ÕÕ¨≈®∂»µƒ—ŒÀ·∑¥”¶
C£ÆΩ´’‚¡Ω÷÷‘™Àÿµƒµ•÷ ∑€ƒ©∑÷±∫Õ»»ÀÆ◊˜”√£¨≤¢µŒ»Î∑”Ù ‘“∫
D£Æ±»Ωœ’‚¡Ω÷÷‘™Àÿµƒ∆¯Ã¨«‚ªØŒÔµƒ»»Œ»∂®–‘
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com