
题目列表(包括答案和解析)
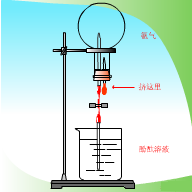 如图所示实验非常有趣,想必给同学们留下了深刻印象.它体现了氨的性质包括( )
如图所示实验非常有趣,想必给同学们留下了深刻印象.它体现了氨的性质包括( )| A、②④ | B、②③ | C、①③④ | D、①④ |
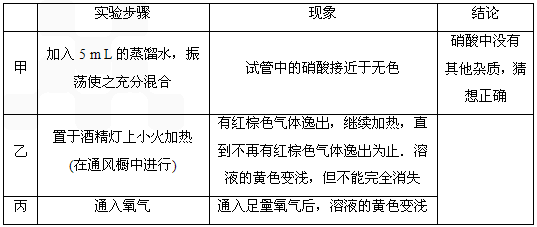
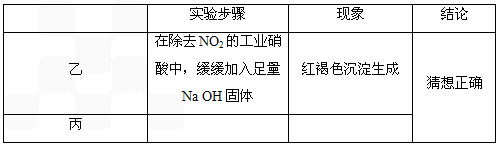
硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量。实验步骤如下:
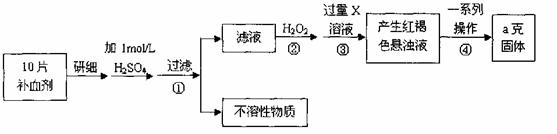
请回答下列问题:
(1))证明步骤①滤液中含有Fe2+的方法是先滴加KSCN溶液,再滴加 ,该过程的现象为: 。
(2)步骤②加入过量H2O2的目的: 。
(3)步骤③中反应的离子方程式: 。
(4)步骤④中一系列处理的操作步骤:过滤、 、灼烧、 、称量。
(5)若实验无损耗,则每片补血剂含铁元素的质量 g。
(6)该小组有些同学认为用KMnO4溶液滴定也能进行铁元素含量的测定。
(5Fe2++MnO4—+8H+=5Fe3++Mn2++4H2O)
①实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、玻棒、烧杯、胶头滴管外,还需
②上述实验中的KMnO4溶液需要酸化,用于酸化的酸是 。
a.稀硝酸 b.稀硫酸 c.盐酸 d.浓硝酸
③滴定到终点时(恰好完全反应)的颜色为 色。k*s5u
某学生在A、B、C、D四支小烧瓶中分别放入干燥的细铁丝、浸过食盐水的细铁丝、浸过清水的细铁丝、食盐水及细铁丝(使细铁丝完全浸没在食盐水中),然后装配成如图所示的四套装置中,每隔一段时间测量导管中水面的高度,结果如下表所示
表中所列数据都为导管水面上升的高度/cm)
时间/小时 | 0 | 0.5 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 |
A瓶(盛干细铁丝) | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
B瓶(盛沾了食盐水的细铁丝) | 0 | 0.4 | 1.2 | 3.4 | 5.6 | 7.6 | 9.8 |
C瓶(盛沾了清水的细铁丝) | 0 | 0 | 0 | 0.3 | 0.8 | 2.0 | 3.5 |
D瓶(细铁丝完全浸没在食盐水中) | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
请回答下列问题:
(1) 导管中水面为什么会上升?
(2) 上述实验中,铁生锈的速率由大到小的顺序为(填小烧瓶的瓶号) 。
影响铁生锈的因素有:

某课外小组做了一个有趣的实验,将2g铝粉和3g碘粉小心混合均匀,分成相等三份,分别进行实验,现将实验记录列表如下:
|
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com