
题目列表(包括答案和解析)
| 熔点 ℃ |
沸点 ℃ |
液态时 密度 g/cm3 |
18℃时在水中的溶解度 mL/L |
乙醚、丙酮 或苯中的 溶解性 |
乙醇 中的 溶解性 |
| -97.73 | -24.2 | 0.9159 | 280 | 互溶 | 能溶 |

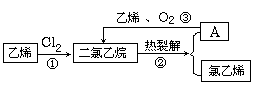
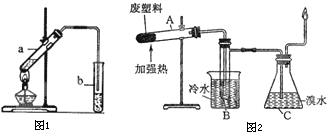
探究一:该小组制备溴乙烷的主要步骤如下:?
①向装置图所示的U形管和大烧杯中加入冷水;?
②在小烧杯中按一定比例配制乙醇、水、浓硫酸混合液;?
③向装置图所示的圆底烧瓶中加入一定量研细的溴化钠和少量碎瓷片;?
④将冷却至室温的混合液转移到圆底烧瓶中,加热;
⑤精制溴乙烷。?

回答下列问题:?
(1)步骤②向乙醇和水缓缓加入浓硫酸时,小烧杯要置于冷水中冷却,除了避免硫酸小液滴飞溅外,更主要的目的是___________________。?
(2)步骤④加热片刻后,烧瓶内的混合物会出现橘红色,出现这种现象的原因是(请用化学方程式表示)_____________________________,改用小火加热后,橘红颜色会逐渐消去,消失的原因是(请用化学方程式表示)__________________________________。?
(3)为了更好地控制反应温度,除按图示小火加热,还可采用的加热方式是________________。
(4)步骤⑤反应结束后,将U形管中的混合物倒入分液漏斗中,静置,待液体分层后,弃去(填“上层”或“下层”)_________液体。为了除去粗产品中的杂质,可用下列试剂中的________(填序号)。
A.氢氧化钠稀溶液
B.碳酸钠稀溶液?
C.硝酸银溶液
D.四氯化碳?
探究二:溴乙烷与NaOH乙醇溶液的反应?
学习小组在进行溴乙烷与NaOH乙醇溶液的反应中,观察到有气体生成。?
请你设计两种不同的方法分别检验该气体,并使用下列简易图标,在答题卡的方框中画出这两种方法的实验装置示意图(所给各种图标,使用次数不限,也可以不全部用),并写出装置中所盛试剂的名称(试剂任选)和实验现象。?


| 实验步骤 | 实验现象 |
| I.向编号为①②③的3支试管中,分别加入1mL 20%的蔗糖溶液,向试管②和③中加入0.5mL稀硫酸,并将这3支试管同时水浴加热约5min | 均无明显现象 |
| II.取试管①和②,加入新制氢氧化铜悬浊液,加热至沸腾 | 均无明显现象 |
| III.取试管③,先加入NaOH溶液调溶液pH至碱性,再加入新制氢氧化铜悬浊液,加热至沸腾 | |
| 结论:证明蔗糖在稀硫酸作用下发生了水解反应 | |
| 产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳 |
| 质量分数(%) | 12 | 24 | 12 | 16 | 20 | 10 | 6 |
苯甲酸甲酯 是一种重要的工业用有机溶剂。请分析下列有机物的结构简式或性质特点,然后回答问题。
是一种重要的工业用有机溶剂。请分析下列有机物的结构简式或性质特点,然后回答问题。

甲 乙
|
丙的分子式 |
C7H8O |
|
丙的部分性质 |
熔融状态下能与钠反应放出氢气 |
|
与乙酸能发生酯化反应 |
(1)乙中含氧官能团的名称是________。
(2)甲、乙、丙三种有机物中与苯甲酸甲酯是同分异构体的是________,在加热条件下能够与新制氢氧化铜悬浊液反应生成红色沉淀的是________,与NaOH溶液在加热条件下反应消耗NaOH最多的是________。

(3)已知:苯在无水AlCl3的作用下与卤代烃发生反应,可以在苯环上增加烷基。
①一定条件下,下列物质不能与A反应的是________(填字母序号)
a.酸性KMnO4溶液 b.溴的CCl4溶液 c.氢气 d.氯气
②丙生成甲的反应类型与________(选填序号)的反应类型相同。
a.反应Ⅰ b.反应Ⅱ c.反应Ⅲ
③写出B生成丙的化学方程式:_________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com