
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
 ШчЭМЮЊЪЕбщЪвФГХЈбЮЫсЪдМСЦПЩЯЕФБъЧЉЃЌЪдИљОнгаЙиЪ§ОнЛиД№ЯТСаЮЪЬт
ШчЭМЮЊЪЕбщЪвФГХЈбЮЫсЪдМСЦПЩЯЕФБъЧЉЃЌЪдИљОнгаЙиЪ§ОнЛиД№ЯТСаЮЪЬт| гІСПШЁХЈбЮЫсЬхЛ§/mL | гІбЁгУШнСПЦПЕФЙцИё/mL |
2.1 2.1 |
250 250 |
ЃЈ14ЗжЃЉгвЭМЮЊЪЕбщЪвФГХЈбЮЫсЪдМСЦПЩЯЕФБъЧЉЃЌЪдИљОнгаЙиЪ§ОнЛиД№ЯТСаЮЪЬт
| |
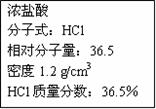
(1)ИУХЈбЮЫсжаHClЕФЮяжЪЕФСПХЈЖШЮЊ__________mol/LЁЃ
(2)ХфжЦ250mL 0.1mol/LЕФбЮЫсШмвК
| гІСПШЁХЈбЮЫсЬхЛ§/mL | гІбЁгУШнСПЦПЕФЙцИё/mL |
|
|
|
AЃЎгУСПЭВСПШЁЫљашЕФХЈбЮЫсЕФЬхЛ§ЃЌбиВЃСЇАєЕЙШыЩеБжаЃЌдйМгШыеєСѓЫЎЃЌгУВЃСЇАєТ§Т§НСЖЏЃЌЪЙЦфЛьКЯОљдШЁЃ
BЃЎНЋвбРфШДЕФбЮЫсбиВЃСЇАєзЂШыШнСПЦПжаЁЃ
CЃЎгУеєСѓЫЎЯДЕг 2ЁЊ3ДЮЃЌЯДЕгвКОљзЂШыШнСПЦПЃЌеёЕДЁЃ
DЃЎМЬајЭљШнСПЦПФкаЁаФМгЫЎЃЌжБЕНвКУцНгНќПЬЖШЯп1~2cmДІЃЌИФгУ МгЫЎЃЌЪЙШмвКАМУцЧЁКУгыПЬЖШЯрЧаЁЃ
EЃЎНЋШнСПЦПИЧНєЃЌеёЕДЃЌвЁдШЁЃ
(3) ШєЪЕбщжаГіЯжЯТСаЯжЯѓЖдЫљХфШмвКХЈЖШгаЪВУДгАЯьЃП(ЬюЦЋИпЁЂЦЋЕЭЁЂЮогАЯь)
ЂйНЋЩеБжаШмвКзЊвЦЕНШнСПЦПжЎЧАЃЌШнСПЦПжагаЩйСПеєСѓЫЎ ЃЛ
ЂкЯђШнСПЦПжазЊвЦШмвКЪБВЛЩїгавКЕЮЕєдкШнСПЦПЭтУцЃЌдђХЈЖШ ЃЛ
ЂлЖЈШнЪБИЉЪгШнСПЦППЬЖШЯп ЁЃ
(4)ЪЕбщЪвРябИЫйжЦБИЩйСПТШЦјПЩРћгУвдЯТЗДгІЃК2 KMnO4+16 HCl === 2 KCl + 2 MnCl2 + 5 Cl2Ёќ+ 8 H2O ДЫЗДгІВЛашвЊМгШШЃЌГЃЮТЯТОЭПЩвдбИЫйНјааЁЃ
ЂйгУЁАЫЋЯпЧХЗЈЁБ БъУїЕчзгзЊвЦЕФЗНЯђКЭЪ§ФПЃК
2 KMnO4+16 HCl === 2 KCl + 2 MnCl2+ 5 Cl2Ёќ + 8 H2O
ЂкгУИУХЈбЮЫсжЦЕУСЫБъПіЯТ560mlCl2,дђБЛбѕЛЏЕФHClЮЊ molЃЌашвЊKMnO4ЕФжЪСП g
ЃЈ14ЗжЃЉгвЭМЮЊЪЕбщЪвФГХЈбЮЫсЪдМСЦПЩЯЕФБъЧЉЃЌЪдИљОнгаЙиЪ§ОнЛиД№ЯТСаЮЪЬт
  |
| гІСПШЁХЈбЮЫсЬхЛ§/mL | гІбЁгУШнСПЦПЕФЙцИё/mL |
| | |
 ДІЃЌИФгУ МгЫЎЃЌЪЙШмвКАМУцЧЁКУгыПЬЖШЯрЧаЁЃ
ДІЃЌИФгУ МгЫЎЃЌЪЙШмвКАМУцЧЁКУгыПЬЖШЯрЧаЁЃ дШЁЃ
дШЁЃ згзЊвЦЕФЗНЯђКЭЪ§ФПЃК
згзЊвЦЕФЗНЯђКЭЪ§ФПЃКЃЈ14ЗжЃЉгвЭМЮЊЪЕбщЪвФГХЈбЮЫсЪдМСЦПЩЯЕФБъЧЉЃЌЪдИљОнгаЙиЪ§ОнЛиД№ЯТСаЮЪЬт
|
|
(1)ИУХЈбЮЫсжаHClЕФЮяжЪЕФСПХЈЖШЮЊ__________mol/LЁЃ
(2)ХфжЦ250mL 0.1mol/LЕФбЮЫсШмвК
|
гІСПШЁХЈбЮЫсЬхЛ§/mL |
гІбЁгУШнСПЦПЕФЙцИё/mL |
|
|
|
AЃЎгУСПЭВСПШЁЫљашЕФХЈбЮЫсЕФЬхЛ§ЃЌбиВЃСЇАєЕЙШыЩеБжаЃЌдйМгШыеєСѓЫЎЃЌгУВЃСЇАєТ§Т§НСЖЏЃЌЪЙЦфЛьКЯОљдШЁЃ
BЃЎНЋвбРфШДЕФбЮЫсбиВЃСЇАєзЂШыШнСПЦПжаЁЃ
CЃЎгУеєСѓЫЎЯДЕг 2ЁЊ3ДЮЃЌЯДЕгвКОљзЂШыШнСПЦПЃЌеёЕДЁЃ
DЃЎМЬајЭљШнСПЦПФкаЁаФМгЫЎЃЌжБЕНвКУцНгНќПЬЖШЯп1~2cmДІЃЌИФгУ МгЫЎЃЌЪЙШмвКАМУцЧЁКУгыПЬЖШЯрЧаЁЃ
EЃЎНЋШнСПЦПИЧНєЃЌеёЕДЃЌвЁдШЁЃ
(3) ШєЪЕбщжаГіЯжЯТСаЯжЯѓЖдЫљХфШмвКХЈЖШгаЪВУДгАЯьЃП(ЬюЦЋИпЁЂЦЋЕЭЁЂЮогАЯь)
ЂйНЋЩеБжаШмвКзЊвЦЕНШнСПЦПжЎЧАЃЌШнСПЦПжагаЩйСПеєСѓЫЎ ЃЛ
ЂкЯђШнСПЦПжазЊвЦШмвКЪБВЛЩїгавКЕЮЕєдкШнСПЦПЭтУцЃЌдђХЈЖШ ЃЛ
ЂлЖЈШнЪБИЉЪгШнСПЦППЬЖШЯп ЁЃ
(4)ЪЕбщЪвРябИЫйжЦБИЩйСПТШЦјПЩРћгУвдЯТЗДгІЃК2 KMnO4+16 HCl === 2 KCl + 2 MnCl2 + 5 Cl2Ёќ + 8 H2O ДЫЗДгІВЛашвЊМгШШЃЌГЃЮТЯТОЭПЩвдбИЫйНјааЁЃ
ЂйгУЁАЫЋЯпЧХЗЈЁБ БъУїЕчзгзЊвЦЕФЗНЯђКЭЪ§ФПЃК
2 KMnO4+16 HCl === 2 KCl + 2 MnCl2 + 5 Cl2Ёќ + 8 H2O
ЂкгУИУХЈбЮЫсжЦЕУСЫБъПіЯТ560mlCl2,дђБЛбѕЛЏЕФHClЮЊ molЃЌашвЊKMnO4ЕФжЪСП g
 ШчЭМЮЊЪЕбщЪвФГХЈбЮЫсЪдМСЦПЩЯЕФБъЧЉЃЌЪдИљОнгаЙиЪ§ОнЛиД№ЯТСаЮЪЬт
ШчЭМЮЊЪЕбщЪвФГХЈбЮЫсЪдМСЦПЩЯЕФБъЧЉЃЌЪдИљОнгаЙиЪ§ОнЛиД№ЯТСаЮЪЬт| гІСПШЁХЈбЮЫсЬхЛ§/mL | гІбЁгУШнСПЦПЕФЙцИё/mL |
| ______ | ______ |
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com