
题目列表(包括答案和解析)
(16分)镁化合物和氯气均具有广泛用途,请回答下列问题:
(1)写镁和氯气反应产物的电子式
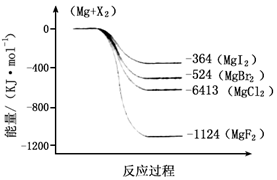
(2)下图是金属镁和卤素反应的能量变化图(反应物和产物均为298K时的稳定状态)。则下列选项中正确的是 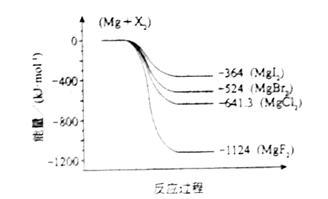
A MgI2中Mg2+与I-间的作用力小于MgF2中Mg2+与F-间的作用力
B Mg与X2的反应是放热反应
C MgBr2与Cl2反应的△H<0
D 化合物的热稳定性顺序为MgI2>MgBr2>MgCl2>MgF2
(3)在298K、100Kpa时,在1L水中可溶解0.09mol氯气,实验测得溶于水的Cl2约有三分之一与水反应。请回答下列问题:
①该反应的离子方程式为 ,平衡常数表达式为
②在上述平衡体系中加入少量NaCl固体,平衡将 (填“正向移动”、“逆向移动”、“不移动”);增大氯气的压强,氯气的溶解度将 ,氯气和水反应的平衡常数将
(填“变大”、“变小”、“不变”)。
③已知: H2CO3 HCO3- + H+ Ka1(H2CO3) = 4.45×10-7
HCO3- + H+ Ka1(H2CO3) = 4.45×10-7
HCO3- CO32- + H+ Ka2(H2CO3) = 5.61×10-11
CO32- + H+ Ka2(H2CO3) = 5.61×10-11
HClO  H+ + ClO- Ka(HClO) = 2.95×10-8
H+ + ClO- Ka(HClO) = 2.95×10-8
请依据以上碳酸和次氯酸的电离平衡常数,写出在下列条件下所发生反应的离子方程式:
将少量的氯气通入到过量的碳酸钠溶液中____________________________________;
(16分)镁化合物和氯气均具有广泛用途,请回答下列问题:
(1)写镁和氯气反应产物的电子式
(2)下图是金属镁和卤素反应的能量变化图(反应物和产物均为298K时的稳定状态)。则下列选项中正确的是
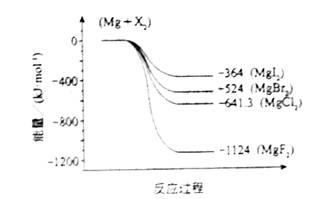
A MgI2中Mg2+与I-间的作用力小于MgF2中Mg2+与F-间的作用力
B Mg与X2的反应是放热反应
C MgBr2与Cl2反应的△H<0
D 化合物的热稳定性顺序为MgI2>MgBr2>MgCl2>MgF2
(3)在298K、100Kpa时,在1L水中可溶解0.09mol氯气,实验测得溶于水的Cl2约有三分之一与水反应。请回答下列问题:
① 该反应的离子方程式为 ,平衡常数表达式为
②在上述平衡体系中加入少量NaCl固体,平衡将 (填“正向移动”、“逆向移动”、“不移动”);增大氯气的压强,氯气的溶解度将 ,氯气和水反应的平衡常数将
(填“变大”、“变小”、“不变”)。
③已知:
H2CO3  HCO3- + H+
Ka1(H2CO3) = 4.45×10-7
HCO3- + H+
Ka1(H2CO3) = 4.45×10-7
HCO3- CO32- + H+
Ka2(H2CO3) = 5.61×10-11
CO32- + H+
Ka2(H2CO3) = 5.61×10-11
HClO  H+ + ClO-
Ka(HClO) = 2.95×10-8
H+ + ClO-
Ka(HClO) = 2.95×10-8
请依据以上碳酸和次氯酸的电离平衡常数,写出在下列条件下所发生反应的离子方程式:
将少量的氯气通入到过量的碳酸钠溶液中____________________________________;
Ⅰ、
氯化铬酰(CrO2Cl2)在有机合成中可作(1)写出铬原子的基态电子排布式________,与铬同周期的所有元素的基态原子中最外层电子数与铬原子相同的元素有________(填元素符号),其中一种金属的晶胞结构如下图所示,该晶胞中含有金属原子的数目为________.
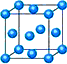
(2)CrO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断CrO2Cl2是________(填“极性”或“非极性”)分子.
(3)在①苯
②CH3OH
③HCHO
④CS2
⑤CCl4
⑥CH3Cl
⑦HCOOH七种有机物质中,碳原子采取sp2杂化的分子有________(填序号),CS2![]() 分子的空间构型是________.
分子的空间构型是________.
Ⅱ、不锈钢是由铁、铬、镍、碳及众多不同元素所组![]() 成的合金.
成的合金.
(1)基![]() 态碳(C)原子的价电子排布式为________.
态碳(C)原子的价电子排布式为________.
(2)[Cr(H2O)4Cl2]Cl·2H2O中Cr3+的配位数为________;[Cr(H2O)4Cl2]Cl中含有的化学键为________.
(3)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,呈四面体构型.423 K时,Ni(CO)4分解为Ni和CO,从而制得高纯度的Ni粉.试推测:四羰基镍的晶体类型是________,Ni(CO)4易溶于________(填序号).
A.水
B.四氯化碳
C.苯
D.硫酸镍溶液
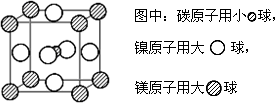
(4)据报道,只含镁、镍和碳三![]() 种元素的晶体竟然具有超导性.鉴于这三种元素都是常见元素,从而引起广泛关注.该晶体的结构可看作由镁原子和镍原子在一起进行面心立方密堆积,试写出该晶体的化学式________.晶体中
种元素的晶体竟然具有超导性.鉴于这三种元素都是常见元素,从而引起广泛关注.该晶体的结构可看作由镁原子和镍原子在一起进行面心立方密堆积,试写出该晶体的化学式________.晶体中![]() 每个镁原子周围距离最近的镍原子有________个.
每个镁原子周围距离最近的镍原子有________个.
 HCO3- + H+ Ka1(H2CO3) = 4.45×10-7
HCO3- + H+ Ka1(H2CO3) = 4.45×10-7  CO32- + H+ Ka2(H2CO3) = 5.61×10-11
CO32- + H+ Ka2(H2CO3) = 5.61×10-11  H+ + ClO- Ka(HClO) = 2.95×10-8
H+ + ClO- Ka(HClO) = 2.95×10-8 四氯化钛(TiCl4)是工业上制备金属钛的重要原料。常温下,它是一种极易水解的无色液体,沸点为136.4℃。工业制备TiCl4和钛的反应分布为:
TiO2 +2C+2Cl2![]() TiCl4 +2CO ;TiCl4 +2Mg
TiCl4 +2CO ;TiCl4 +2Mg Ti + 2MgCl2
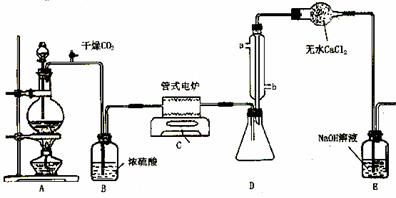
下图是实验室制备TiCl4的反应装置,主要操作步骤:
①连接好整套装置,在通Cl2前先通入CO2气体并持续一段时间;
②当锥形瓶中TiCl4的量不再增加时,停止加热,从侧管中改通CO2气体直到电炉中的瓷管冷却为止;
③将TiO2、炭粉混合均匀后,装入管式电炉中;
④ 将电炉升温到800℃,一段时间后改通Cl2,同时在冷凝管中通冷凝水。
试回答下列问题:
⑴.正确的操作顺序为(填序号)___________________________。
⑵.装置A中的反应的离子方程式为__________________________。
⑶.操作①的目的是_________________________________。
⑷.装置D中冷凝管进水口的位置是(填a或b)_________,
装置E的作用是___________________________________________________。
⑸.TiCl4露置于空气中极易水解,其化学方程式可表示为_____________________。
⑹.工业上常用金属镁在800℃高温和氩气氛围中还原TiCl4的方法制备钛,
![]() ,氩气的作用为_____________________________.
,氩气的作用为_____________________________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com