
题目列表(包括答案和解析)
(15分)
在常温下,某水溶液M中。
(1)若M中存在的离子只有:Na+、CH3COO-、H+、OH-,下列关系合理的是 。
① c(Na+)>c(CH3COO-)>c(OH-)>c(H+) ② c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
③ c(H+)>c(OH-)>c(Na+)>c(CH3COO-) ④ c(Na+)=c(CH3COO-)且c(OH-)=c(H+)
(2)若M由两种相同物质的量浓度的溶液混合而成,其中只存在OH—、H+、NH4+、Cl-四种离子,且c(NH4+)>c(Cl-)>c(OH—)>c(H+),这两种溶液的溶质是 。
(3)若M为0.01 mol/L的氨水,向其中加入等体积pH=2的盐酸溶液(忽略溶液体积变化),所得混合液中:c(NH4+)+c(H+)-c(OH-)= 。
(4)若M为20 mL稀硫酸和盐酸混合液,向该混合酸溶液中逐滴加入pH=13的Ba(OH)2溶液,生成BaSO4的量如图所示,当加入60 mLBa(OH)2溶液时,C点溶液的pH=7(忽略溶液体积变化),试计算:
(i)最初混合酸溶液中c(H2SO4)=__________,c(HCl)=____________。
(ii)B点溶液的pH为多少?(写出计算过程。可能用到的数据:1g2=0.30、1g3=0.48)
在常温下,某水溶液M中。
(1)若M中存在的离子只有:Na+、CH3COO-、H+、OH-,下列关系合理的是 。
① c(Na+)>c(CH3COO-)>c(OH-)>c(H+) ② c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
③ c(H+)>c(OH-)>c(Na+)>c(CH3COO-) ④ c(Na+)=c(CH3COO-)且c(OH-)=c(H+)
(2)若M由两种相同物质的量浓度的溶液混合而成,其中只存在OH—、H+、NH4+、Cl-四种离子,且c(NH4+)>c(Cl-)>c(OH—)>c(H+),这两种溶液的溶质是 。
(3)若M为0.01 mol/L的氨水,向其中加入等体积pH=2的盐酸溶液(忽略溶液体积变化),所得混合液中:c(NH4+)+c(H+)-c(OH-)= 。
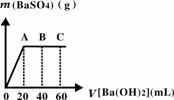 (4)若M为20 mL稀硫酸和盐酸混合液,向该混合酸溶液
(4)若M为20 mL稀硫酸和盐酸混合液,向该混合酸溶液
中逐滴加入pH=13的Ba(OH)2溶液,生成BaSO4的量
如右图所示,当加入60 mL Ba(OH)2溶液时,C点溶液
的pH=7(忽略溶液体积变化),试计算:
(i)最初混合酸溶液中c(H2SO4)=__________,c(HCl)=____________。
(ii)B点溶液的pH为多少?(写出计算过程。可能用到的数据:1g2=0.30、1g3=0.48)
(13分)现有浓度为0.1 mol?L-1的五种电解质溶液: ① Na2CO3 ② NaHCO3 ③ NaAlO2 ④ CH3COONa ⑤ NaOH
已知:CO2+3H2O+2AlO2-===2Al(OH)3↓+CO32-
(1)这五种溶液的pH由小到大的顺序是___ ___(填编号);
(2)将五种溶液稀释相同的倍数时,其pH变化最大的是____ __(填编号);
(3)混合碳酸(H2CO3)溶液和NaAlO2溶液,试写出可能发生的化学反应方程式:
;
(4)常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
实验编号 | HA物质的量浓度(mol/L) | NaOH物质的量浓度(mol/L) | 混合溶液的pH |
甲 | 0.20 | 0.20 | pH=a |
乙 | 0.10 | 0.10 | pH=8.00 |
不考虑乙组的实验结果,单从甲组情况分析,如何用a(混合溶液的pH)来说明HA是强酸还是弱酸 ;
乙组实验所得混合溶液中由水电离出的c (OH-)= mol/L。
求出该混合溶液中下列算式的值,要求写出推理、计算过程。
I.c (Na+)-c (A-): ;
Ⅱ.c (OH-)-c (HA): 。
结合下表回答下列问题(均为常温下的数据):
| 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) |
| CH3COOH | 1.8×10-5 | H2CO3 | K1=4.4×10-7 K2=4.7×10-11 |
| HClO | 3×10-8 |
| 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) |
| CH3COOH | 1.8×10-5 | H2CO3 | K1=4.4×10-7 K2=4.7×10-11 |
| HClO | 3×10-8 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com