
题目列表(包括答案和解析)
 CH3OH(g)+H2O(g) △H=-49.0 kJ/mol。测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。从反应开始到平衡,氢气的反应速率v(H2)=
CH3OH(g)+H2O(g) △H=-49.0 kJ/mol。测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。从反应开始到平衡,氢气的反应速率v(H2)=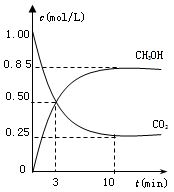

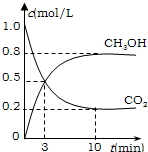 为减小CO2对环境的影响,在限制其排放量的同时,应加强对CO2创新利用的研究.
为减小CO2对环境的影响,在限制其排放量的同时,应加强对CO2创新利用的研究.| 1 |
| 2 |
| 溶解度(S)/g | 溶度积(Ksp) | ||
| Ca(OH)2 | Ba(OH)2 | CaCO3 | BaCO3 |
| 0.16 | 3.89 | 2.9×10-9 | 2.6×10-9 |
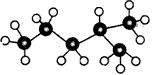
 此烷烃的一溴代物有___________种。
此烷烃的一溴代物有___________种。(本题共12分)
下图是某化学兴趣小组进行丁烷裂解的实验流程。(注:CuO能将烃氧化成CO2和H2O,G后面装置与答题无关,省略铁架台等。)按下图连好装置后,需进行的实验操作有:①给D、G装置加热;②检查整套装置的气密性;③排出装置中的空气等……
(1)这三步操作的先后顺序依次是 (写编号);
(2)简要说明排空气的方法和证明空气已排尽的方法 ;
(3)B装置所起的作用是 ;
(4)假定丁烷按C4H10→C2H6+C2H4和C4H10→CH4+C3H6的方式完全裂解,当(E+F)装置的总质量比反应前增加了0.7g,G装置的质量减少了1.76g,则丁烷的裂解产物中,甲烷与乙烷的物质的量之比为 。(假定流经D、G装置中的气体能完全反应)
若对E装置中的混合物再按以下流程实验: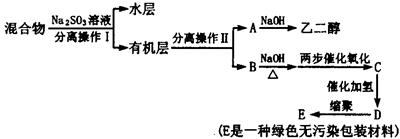
(5)分离操作Ⅰ和Ⅱ的名称分别是:Ⅰ Ⅱ ,Na2SO3溶液的作用是(用离子方程式表示) 。
(6)D的结构简式是 。
(本题共12分)
下图是某化学兴趣小组进行丁烷裂解的实验流程。(注:CuO能将烃氧化成CO2和H2O,G后面装置与答题无关,省略铁架台等。)按下图连好装置后,需进行的实验操作有:①给D、G装置加热;②检查整套装置的气密性;③排出装置中的空气等……
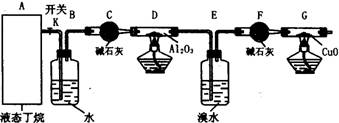
(1)这三步操作的先后顺序依次是 (写编号);
(2)简要说明排空气的方法和证明空气已排尽的方法 ;
(3)B装置所起的作用是 ;
(4)假定丁烷按C4H10→C2H6+C2H4和C4H10→CH4+C3H6的方式完全裂解,当(E+F)装置的总质量比反应前增加了0.7g,G装置的质量减少了1.76g,则丁烷的裂解产物中,甲烷与乙烷的物质的量之比为 。(假定流经D、G装置中的气体能完全反应)
若对E装置中的混合物再按以下流程实验:
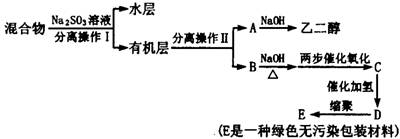
(5)分离操作Ⅰ和Ⅱ的名称分别是:Ⅰ Ⅱ ,Na2SO3溶液的作用是(用离子方程式表示) 。
(6)D的结构简式是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com