
题目列表(包括答案和解析)
(13分)Ⅰ.某学校研究性学习小组开展“不同条件对化学反应速率影响的探究”课题,选用4 mL 0.01 mol·L-1KMnO4溶液与2 mL 0.1 mol·L-1 H2C2O4溶液进行实验,改变条件如下:
| 组别 | 10%硫酸的体积(mL) | 温度/℃ | 其他物质 |
| ① | 2 mL | 20 | |
| ② | 2 mL | 20 | 10滴饱和MnSO4溶液 |
| ③ | 2 mL | 30 | |
| ④ | 1 mL | 20 | 1 mL蒸馏水 |
(13分)Ⅰ.某学校研究性学习小组开展“不同条件对化学反应速率影响的探究”课题,选用4 mL 0.01 mol·L-1KMnO4溶液与2 mL 0.1 mol·L-1 H2C2O4溶液进行实验,改变条件如下:
|
组别 |
10%硫酸的体积(mL) |
温度/℃ |
其他物质 |
|
① |
2 mL |
20 |
|
|
② |
2 mL |
20 |
10滴饱和MnSO4溶液 |
|
③ |
2 mL |
30 |
|
|
④ |
1 mL |
20 |
1 mL蒸馏水 |
(1)如果研究催化剂对化学反应速率的影响,使用实验 和 (用①~④表示,下同);如果研究温度对化学反应速率的影响,使用实验 和 。
(2)对比实验①和④,可以研究 对化学反应速率的影响,实验④中加入1 mL蒸馏水的目的是 。
Ⅱ.该小组查阅资料得知:C2O42-+MnO4-+H+→ CO2↑+Mn2++H2O(未配平),欲利用该反应测定某草酸钠(Na2C2O4)样品中草酸钠的质量分数。该小组称量1.34 g草酸钠样品溶于稀硫酸中,然后用0.200 mol·L-1的酸性高锰酸钾溶液进行滴定(其中的杂质不跟高锰酸钾和稀硫酸反应)。
(1)滴定前是否要滴加指示剂? (填“是”或“否”),请说明理由 。
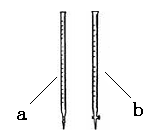
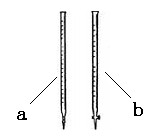
(2)滴定时用 (填a或b)滴定管盛装KMnO4标准溶液。

(3)达到终点时消耗了15.00 mL的高锰酸钾溶液,样品中草酸钠的质量分数为 。
某校研究性学习小组的同学学习完氮的有关物质的性质之后,对氮元素的氢化物NH3性质的探究。
(1)实验室制取氨气的化学方程式为 。
(2)某同学模仿排饱和食盐水收集氯气的方法,想用排饱和氯化铵溶液的方法收集氨气。你认为他能否达到目的? (填“能”或“否”),理由是
。
(3)该小组的同学设计了如图所示的实验装置(夹持及尾气处理装置未画出),探究氨气的还原性。
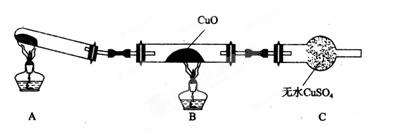
①该装置在设计上有一定缺陷。为保证实验结果的准确性,对该装置的改进措施是
。
②利用改进后的装置进行实验,CuO变为红色物质,无水CuSO4变蓝,同时生成一种无污染的气体。氨气与CuO反应的化学方程式为 。
③有同学认为NH3与CuO反应生成的红色物质中可能含Cu2O。Cu2O在酸性溶液中Cu+歧化生成Cu和Cu2+。请设计一个简单的实验检验该红色物质中是否含有Cu2O
。
| 组别 | 10%硫酸的体积(mL) | 温度/℃ | 其他物质 |
| ① | 2 mL | 20 | |
| ② | 2 mL | 20 | 10滴饱和MnSO4溶液 |
| ③ | 2 mL | 30 | |
| ④ | 1 mL | 20 | 1 mL蒸馏水 |
(9分)某校研究性学习小组的同学学习完氮的有关物质的性质之后,对氮元素的氢化物NH3性质的探究。
(1)实验室制取氨气的化学方程式为 。
(2)某同学模仿排饱和食盐水收集氯气的方法,想用排饱和氯化铵溶液的方法收集氨气。你认为他能否达到目的? (填“能”或“否”),理由是 。
(3)该小组的同学设计了如图所示的实验装置(夹持及尾气处理装置未画出),探究氨气的还原性。
①该装置在设计上有一定缺陷。为保证实验结果的准确性,对该装置的改进措施是
。
②利用改进后的装置进行实验,CuO变为红色物质,无水CuSO4变蓝,同时生成一种无污染的气体。氨气与CuO反应的化学方程式为 。
③有同学认为NH3与CuO反应生成的红色物质中可能含Cu2O。Cu2O在酸性溶液中Cu+歧化生成Cu和Cu2+。请设计一个简单的实验检验该红色物质中是否含有Cu2O
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com