实验室合成乙酸乙酯时,得到乙酸乙酯粗产品.请回答下列问题:
(已知:乙醇、乙酸、乙酸乙酯的沸点依次是78.4℃、118℃、77.1℃)
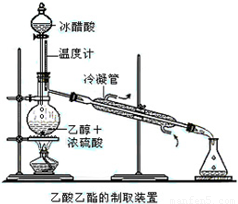
(1)在烧瓶中除了加入______、______、______外,还应放入几块碎瓷片,其目的是防止烧瓶中液体暴沸.
(2)在烧瓶中加入一定比例的乙醇和浓硫酸的混合液的方法是:______.
(3)生成乙酸乙酯的反应是可逆反应,反应物不能完全转化为生成物,反应一段时间后,就达到了该反应的限度,当达到化学平衡状态时:(填序号)______.
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
④正反应的速率与逆反应的速率相等 ⑤混合物中各物质的浓度不再变化
(4)现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,下图是分离操作步骤流程图.请在图中圆括号内填入适当的试剂,在方括号内填入适当的分离方法.
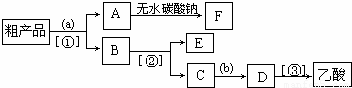
E为______(填名称);试剂a是______,试剂b为______;分离方法①是______,分离方法②是______.
(5)写出合成乙酸乙酯反应的化学方程式______


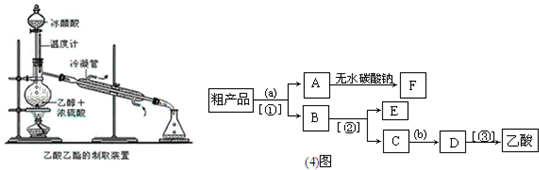


 实验室合成乙酸乙酯时,得到乙酸乙酯粗产品.请回答下列问题:
实验室合成乙酸乙酯时,得到乙酸乙酯粗产品.请回答下列问题:
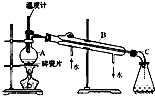 (1)实验室分馏石油的正确操作顺序是:A→
(1)实验室分馏石油的正确操作顺序是:A→