
题目列表(包括答案和解析)

(1)A中浓硫酸的作用是___________________________;若用同位素18O示踪法确定反应产物水分子中氧原子的提供者,写出能表示18O位置的化学方程式:______________________。
(2)球形管C的作用是__________________________,若反应前向B中溶液滴加几滴酚酞,呈红色,产生此现象的原因是(用离子方程式表示)___________________________;反应结束后B中的现象是___________________________________。
(3)从B中分离出的乙酸乙酯中还含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,过滤分离出___________________________;再加入无水硫酸钠,然后进行蒸馏,收集温度为__________________馏分,以得到较纯净的乙酸乙酯。
(4)试分析用氢氧化钠溶液来代替饱和碳酸钠溶液而导致的不利后果。__________________。
| |||||||||||||||||||
(1)A中浓硫酸的作用是______________;若用同位素18O示踪法确定反应产物水分子中氧原子的提供者,写出能表示18O位置的化学方程式:______________.
(2)球型管C的两个作用是________、________,若反应前向B中溶液滴加几滴酚酞,呈红色,产生此现象的原因是(用离子方程式表示)_______________;反应结束后B中的现象是_______________.
(3)从B中分离出的乙酸乙酯中还含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,过滤分离出________;再加入无水硫酸钠,然后进行蒸馏,收集77℃左右的馏分,以得到较纯净的乙酸乙酯.
(4)试分析用氢氧化钠溶液来代替饱和碳酸钠溶液而导致的不利后果.
_____________________________________________________________________
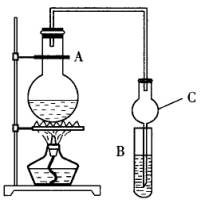
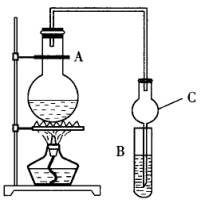
某课外活动小组设计的实验室制取较多量乙酸乙酯的装置如下图所示,A中放有乙醇、无水醋酸钠和浓硫酸,B中放有饱和碳酸钠溶液(已知①无水CaCl2可与乙醇形成难溶于水的CaCl2·6C6H5OH;②有关有机物的沸点,乙醚:34.7℃;乙醇:78.5℃;乙酸118℃;乙酸乙酯77.1℃),试回答:
(1)A中浓硫酸的作用是______________;若用同位素18O示踪法确定反应产物水分子中氧原子的提供者,写出能表示18O位置的化学方程式:______________.
(2)球型管C的两个作用是________、________,若反应前向B中溶液滴加几滴酚酞,呈红色,产生此现象的原因是(用离子方程式表示)_______________;反应结束后B中的现象是_______________.
(3)从B中分离出的乙酸乙酯中还含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,过滤分离出________;再加入无水硫酸钠,然后进行蒸馏,收集77℃左右的馏分,以得到较纯净的乙酸乙酯.
(4)试分析用氢氧化钠溶液来代替饱和碳酸钠溶液而导致的不利后果.
_____________________________________________________________________

①设计甲装置的目的是_________________。甲装置__________(填“能”或“不能”)用乙装置来代替。
②装置乙中盛有的液体是__________,该装置可看作是一个___________(填某仪器名称)。
(2)在氮的化合物中,有一类盐叫亚硝酸盐,如亚硝酸钠(NaNO2)等。NaNO2是一种潜在的致癌物质,过量或长期使用会对人产生危害。由于亚硝酸钠有咸味,外观与NaCl相似,曾多次发生过被误当食盐使用的事件。已知:HNO2是一种弱酸,不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把I-氧化成I2;AgNO2是一种难溶于水易溶于酸的化合物。试回答下列问题:
①人体正常的血红蛋白中应含Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是_____________。
A.亚硝酸盐是还原剂 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐被还原
②下列说法中,能用来区别NaNO2和NaCl的是______________。
A.测定这两种溶液的pH
B.用AgNO3和HNO3两种试剂来区别
C.在酸性条件下加入KI淀粉试液来区别
③把新制氯气通入到NaNO2溶液中,氯水褪色,生成NaNO3和HCl,请写出此反应的离子方程式______________。
④为了测定某样品中NaNO2的含量,可以使用标准?KMnO4?溶液进行滴定,试回答:KMnO4溶液在滴定过程中作____________(填“氧化剂”或“还原剂”),该滴定过程_____________(填“要”或“不要”)另加指示剂。
⑤已知HNO2的酸性比醋酸略强,某同学在家中进行鉴别NaNO2与NaCl的实验,但他家中只有浓醋酸,请问该实验能否成功?____________(填“能”或“不能”),请说明理由_______
_____________________________________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com