
题目列表(包括答案和解析)
 (2013?临沂一模)【化学--物质结构与性质】
(2013?临沂一模)【化学--物质结构与性质】| 160 |
| a3b |
| 160 |
| a3b |
 有A、B、C、D、E、M、X七种元素.其相关信息如下:
有A、B、C、D、E、M、X七种元素.其相关信息如下:| 相关信息 | |
| ① | A的基态原子2p轨道中有三个未成对电子 |
| ② | A、B元素的常见单质是构成空气的主要成分 |
| ③ | C是电负性最大的元素 |
| ④ | D是主族元素,基态原子有四个能层,且最外能层上只有两个电子 |
| ⑤ | D、E、M、X四种元素处于同一周期; M与E又位于同一族,M的原子序数比E多1,M的基态原子中含有三个未成对电子; X原子外围电子排布式为3d104s1 |
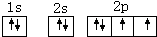

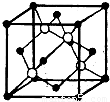
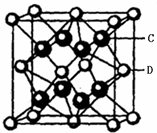
某离子化合物的晶胞如右图所示立体结构,晶胞是整个晶体中最基本的重复单位。阳离子位于此晶胞的中心,阴离子位于8个顶点,该离子化合物中,阴、阳离子个数比是( )

A.1∶8 B.1∶4 C.1∶2 D.1∶1
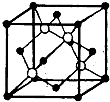
如右图所示为冰的一种骨架形式,依此为单位向空间延伸,那么该冰中的每个水分子氢键个数为
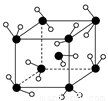
A.1 B.3 C.2 D.4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com