针对苏教版化学1第75页上“铁与氧化性较弱的氧化剂(如盐酸、硫酸铜溶液等)反应转化为+2价铁的化合物,如果与氧化性较强的氧化剂(如氯气、双氧水等)反应则转化为+3价的化合物”的叙述,化学研究性学习小组拟通过以下实验探究“新制的还原性铁粉和盐酸的反应(铁过量)”.请你参与探究并回答有关问题:
(1)利用KSCN、H
2O
2等药品检验反应后的混合液中含有二价铁的实验方法和现象是
先加硫氰化钾溶液,无现象,再滴加双氧水少许,看到溶液呈血红色
先加硫氰化钾溶液,无现象,再滴加双氧水少许,看到溶液呈血红色
;但在实验中往往又看到红色迅速褪去,同时溶液呈黄色,其可能的原因是
硫氰根被氧化
硫氰根被氧化
;学生在做实验时往往滴加双氧水的浓度过大,或者过量,还看到迅速产生大量气泡,写出该现象产生的化学方程式:
.
(2)有资料介绍“取少量反应液(含二价铁)先滴加少量新制饱和氯水,然后滴加KSCN溶液,呈现血红色.若再滴加过量新制氯水,却发现红色褪去.同学对红色褪去的原因提出各自的假设.某同学的假设是:溶液中的+3价铁被氧化为更高的价态.”如果+3价铁被氧化为FeO
42-,试写出该反应的离子方程式
2Fe3++3Cl2+8H2O═2FeO42-+6Cl-+16H+
2Fe3++3Cl2+8H2O═2FeO42-+6Cl-+16H+
.
(3)探究高铁酸钾的某种性质.
【实验一】将适量K
2FeO
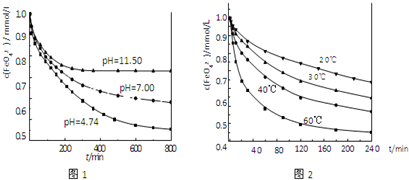
4固体分别溶解于pH 为 4.74、7.00、11.50 的水溶液中,配得FeO
42-浓度为 1.0mmol?L
-1(1mmol?L
-1=10
-3mol?L
-1)的试样,静置,考察不同初始 pH 的水溶液对K
2FeO
4某种性质的影响,结果见图1(注:800min后,三种溶液中高铁酸钾的浓度不再改变).
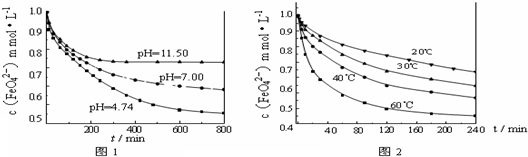

【试验二】将适量 K
2FeO
4溶解于pH=4.74 的水溶液中,配制成FeO
42-浓度为 1.0mmol?L
-1 的试样,将试样分别置于 20℃、30℃、40℃和 60℃的恒温水浴中,考察不同温度对K
2FeO
4某种性质的影响,结果见图2.则
①实验1的目的是
研究FeO42-在不同pH溶液中的稳定性(或反应的速率)
研究FeO42-在不同pH溶液中的稳定性(或反应的速率)
;
②实验2可得出的结论是
温度越高,FeO42-越不稳定(或与水反应的速率越快)
温度越高,FeO42-越不稳定(或与水反应的速率越快)
;
③高铁酸钾在水中的反应为4FeO
42-+10H
2O?4Fe(OH)
3+8OH
-+3O
2↑.由图1可知,800min时,pH=11.50的溶液中高铁酸钾最终浓度比pH=4.74的溶液中高,主要原因是
pH=11.50的溶液中OH-离子浓度大,使平衡向左移动
pH=11.50的溶液中OH-离子浓度大,使平衡向左移动
.

 某校高一化学研究性学习小组对日常生活中的氯气用途进行了调查,了解到氯气可广泛地应用于衣物的漂白、水体的杀菌和消毒等.
某校高一化学研究性学习小组对日常生活中的氯气用途进行了调查,了解到氯气可广泛地应用于衣物的漂白、水体的杀菌和消毒等.