
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
“—÷™ÃÏ»ª∆¯µƒ÷˜“™≥…∑÷ «“ª÷÷ª·≤˙…˙Œ¬ “–ß”¶µƒ∆¯Ã£¨µ»ŒÔ÷ πª¡øµƒ
«“ª÷÷ª·≤˙…˙Œ¬ “–ß”¶µƒ∆¯Ã£¨µ»ŒÔ÷ πª¡øµƒ ∫Õ
∫Õ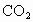 ≤˙…˙µƒŒ¬ “–ß”¶£¨«∞’þ¥Û£¨œ¬√Ê”–πÿÃÏ»ª∆¯µƒº∏÷÷– ˆ÷–’˝»∑µƒ «
≤˙…˙µƒŒ¬ “–ß”¶£¨«∞’þ¥Û£¨œ¬√Ê”–πÿÃÏ»ª∆¯µƒº∏÷÷– ˆ÷–’˝»∑µƒ «
¢ŸÃÏ»ª∆¯”Î√∫°¢≤Ò”Õœý±» «Ωœ«ÂΩýµƒƒÐ‘¥
¢⁄µ»÷ ¡øµƒ ∫Õ
∫Õ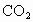 ≤˙…˙µƒŒ¬ “–ß”¶“≤ ««∞’þ¥Û
≤˙…˙µƒŒ¬ “–ß”¶“≤ ««∞’þ¥Û
¢€»º…’ÃÏ»ª∆¯“≤ «À·”͵ƒ≥…“Ú÷Æ“ª
[°°°°]
“—÷™ÃÏ»ª∆¯µƒ÷˜“™≥…∑÷ «“ª÷÷ª·≤˙…˙Œ¬ “–ß”¶µƒ∆¯Ã£¨µ»ŒÔ÷ πª¡øµƒ
«“ª÷÷ª·≤˙…˙Œ¬ “–ß”¶µƒ∆¯Ã£¨µ»ŒÔ÷ πª¡øµƒ ∫Õ
∫Õ ≤˙…˙µƒŒ¬ “–ß”¶£¨«∞’þ¥Û£¨œ¬√Ê”–πÿÃÏ»ª∆¯µƒº∏÷÷– ˆ÷–’˝»∑µƒ «
≤˙…˙µƒŒ¬ “–ß”¶£¨«∞’þ¥Û£¨œ¬√Ê”–πÿÃÏ»ª∆¯µƒº∏÷÷– ˆ÷–’˝»∑µƒ «
¢ŸÃÏ»ª∆¯”Î√∫°¢≤Ò”Õœý±» «Ωœ«ÂΩýµƒƒÐ‘¥
¢⁄µ»÷ ¡øµƒ ∫Õ
∫Õ ≤˙…˙µƒŒ¬ “–ß”¶“≤ ««∞’þ¥Û
≤˙…˙µƒŒ¬ “–ß”¶“≤ ««∞’þ¥Û
¢€»º…’ÃÏ»ª∆¯“≤ «À·”͵ƒ≥…“Ú÷Æ“ª
[°°°°]




| ||
| ||
| ||
| ||
| 5b |
| a-b |
| 5b |
| a-b |
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com