
题目列表(包括答案和解析)
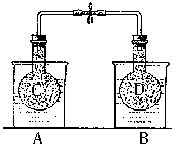 NO2和N2O4的混合气体盛在两个连通的烧瓶C、D里,然后用夹子夹住橡皮管,把烧瓶C放人A烧杯中,烧瓶D放人B烧杯中。
NO2和N2O4的混合气体盛在两个连通的烧瓶C、D里,然后用夹子夹住橡皮管,把烧瓶C放人A烧杯中,烧瓶D放人B烧杯中。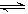 N2O4(g)
N2O4(g)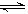 2NO2(g)达到化学平衡状态时压强变为1.515×105Pa,则平衡混合气体的平均相对分子质量为___________(精确到小数点后两位)。
2NO2(g)达到化学平衡状态时压强变为1.515×105Pa,则平衡混合气体的平均相对分子质量为___________(精确到小数点后两位)。
| |||||||||||||||||||||||
A.等于5 s B.等于10 s
C.大于10 s D.小于10 s
将9.2 g N2O4晶体放入容积为2 L的密闭容器中,升温到25℃时N2O4全部气化,由于N2O4发生如下分解反应:
N2O4(g)平衡后,在25℃时测得混合气体(N2O4和NO2)的压强为同温下N2O4(g)尚未分解时压强的1.2倍.试回答:
(1)平衡时容器内NO2和N2O4的物质的量之比为________.
(2)平衡时该反应的化学平衡常数K为________.
(3)如果改变该可逆反应的下列条件,则平衡常数是否改变?
①加压:________;
②升高温度:________;
③增大N2O4的浓度:________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com