
题目列表(包括答案和解析)
已知下列各组热化学方程式:
(1)Fe2O3(s)+3CO(g)![]() 2Fe(s)+3CO2 ΔH1=-26.7 kJ/mol ①
2Fe(s)+3CO2 ΔH1=-26.7 kJ/mol ①
(2)3Fe2O3(s)+CO(g)![]() 2Fe3O4(s)+CO2(g) ΔH2=-50.57 kJ/mol ②
2Fe3O4(s)+CO2(g) ΔH2=-50.57 kJ/mol ②
(3)Fe3O4(s)+CO(g)![]() 3FeO(s)+CO2(g) ΔH3=-36.5 kJ/mol ③
3FeO(s)+CO2(g) ΔH3=-36.5 kJ/mol ③
试求出FeO(s)+CO(g)![]() Fe(s)+CO2(g)的反应热 ΔH.
Fe(s)+CO2(g)的反应热 ΔH.
(10分)试回答下列各问题:
(1)如图Ⅰ所示是1 mol NO2和CO反应生成 CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式: 。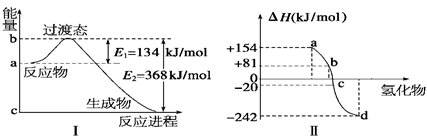
(2)化学反应的焓变与反应物和生成物的键能有关。
①已知:H2(g)+Cl2(g) ="==" 2HCl(g) ΔH="-185" kJ/mol;
键能ΔH298(H—H)="436" kJ/mol,ΔH298(Cl—Cl)="247" kJ/mol,则ΔH298(H—Cl)= 。
②图Ⅱ表示氧族元素中的氧、硫、硒(Se)、碲生成氢化物时的焓变数据,根据这组焓变数据可确定a、b、c、d分别代表的元素,试写出硒化氢发生分解反应的热化学方程式: 。
(3)已知: ①Fe2O3(s)+3CO(g)  2Fe(s)+3CO2(g) ΔH="-a" kJ/mol
2Fe(s)+3CO2(g) ΔH="-a" kJ/mol
②3Fe2O3(s)+CO(g)  2Fe3O4(s)+CO2(g) ΔH="-b" kJ/mol
2Fe3O4(s)+CO2(g) ΔH="-b" kJ/mol
③Fe3O4(s)+CO(g)  3FeO(s)+CO2(g) ΔH="+ckJ/mol"
3FeO(s)+CO2(g) ΔH="+ckJ/mol"
则FeO(s) +CO(g)  Fe(s)+CO2(g) ΔH=- 。
Fe(s)+CO2(g) ΔH=- 。
(10分)试回答下列各问题:
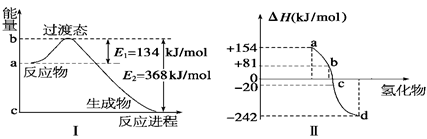
(1)如图Ⅰ所示是1 mol NO2和CO反应生成 CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式: 。
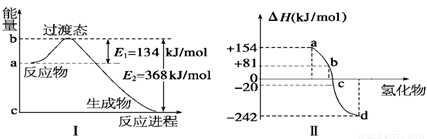
(2)化学反应的焓变与反应物和生成物的键能有关。
①已知:H2(g)+Cl2(g) === 2HCl(g) ΔH=-185 kJ/mol;
键能ΔH298(H—H)=436 kJ/mol,ΔH298(Cl—Cl)=247 kJ/mol,则ΔH298(H—Cl)= 。
②图Ⅱ表示氧族元素中的氧、硫、硒(Se)、碲生成氢化物时的焓变数据,根据这组焓变数据可确定a、b、c、d分别代表的元素,试写出硒化氢发生分解反应的热化学方程式: 。
(3)已知: ①Fe2O3(s)+3CO(g)
 2Fe(s)+3CO2(g) ΔH=-a
kJ/mol
2Fe(s)+3CO2(g) ΔH=-a
kJ/mol
②3Fe2O3(s)+CO(g)
 2Fe3O4(s)+CO2(g)
ΔH=-b kJ/mol
2Fe3O4(s)+CO2(g)
ΔH=-b kJ/mol
③Fe3O4(s)+CO(g)
 3FeO(s)+CO2(g) ΔH=+ckJ/mol
3FeO(s)+CO2(g) ΔH=+ckJ/mol
则FeO(s) +CO(g)  Fe(s)+CO2(g) ΔH=-
。
Fe(s)+CO2(g) ΔH=-
。
 2Fe(s)+3CO2(g) ΔH="-a" kJ/mol
2Fe(s)+3CO2(g) ΔH="-a" kJ/mol 2Fe3O4(s)+CO2(g) ΔH="-b" kJ/mol
2Fe3O4(s)+CO2(g) ΔH="-b" kJ/mol  3FeO(s)+CO2(g) ΔH="+ckJ/mol"
3FeO(s)+CO2(g) ΔH="+ckJ/mol"  Fe(s)+CO2(g) ΔH=- 。
Fe(s)+CO2(g) ΔH=- 。湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com