A、B、C、D、E、W均为短周期元素,原子序数依次增大.回答下列问题:
(1)E单质为双原子分子,气体E的密度3.17g.L
-1(标准状况),写出用石灰水吸收E反应的离子方程式:
Cl2+2OH-=Cl-+ClO-+2H2O
Cl2+2OH-=Cl-+ClO-+2H2O
(2)由A、B、D元素原子组成的化合物CH
4和H
2O在一定条件下发生反应:CH
4(g)+H
2O(g)CO(g)+3H
2(g).将1.0mol CH
4和2.0mol H
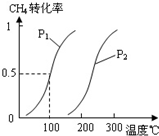
2O(g)通入反应室(容积为100L),达到平衡时,CH
4的转化率与温度、压强的关系如图.
①已知100℃时达到平衡所需的时间为5min,则用H
2表示的平均反应速率为
0.0030mol?L-1?min-1
0.0030mol?L-1?min-1
.
②图中的P
1<
<
P
2(填“<”、“>”或“=”),100℃时平衡常数为
2.25×10-4
2.25×10-4
.
③在其它条件不变的情况下降低温度,逆反应速率将
减小
减小
(填“增大”、“减小”或“不变”).
(3)由A、C、D元素原子组成的化合物N
2H
4和H
2O
2有广泛的用途.
①N
2H
4(肼)一空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的氢氧化钾溶液.电池放电时,负极的电极反应式为
N2H4+4OH-=N2↑+4H2O+4e-
N2H4+4OH-=N2↑+4H2O+4e-
.
②已知:16g液态N
2H
4(肼)与足量过氧化氢反应生成氮气和水蒸气,放出320.75KJ的热量.
H
2O(1)=H
2O(g)△H=+44kJ?mol
-12H
2O
2(1)=2H
2O(1)+O
2(g)△H=-196.4kJ?mol
-1写出N
2H
4(肼)与氧气反应的热化学方程式为
N2H4(1)+O2(g)=N2(g)+2H2O(1)△H=-621.1kJ?mol-1
或N2H4(1)+O2(g)=N2+2H2O(g)△H=-533.1kJ?mol-1
N2H4(1)+O2(g)=N2(g)+2H2O(1)△H=-621.1kJ?mol-1
或N2H4(1)+O2(g)=N2+2H2O(g)△H=-533.1kJ?mol-1
.

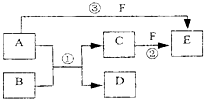 A、B、C、D、E、F六种物质的相互转化关系如下图所示(反应条件未标出),
A、B、C、D、E、F六种物质的相互转化关系如下图所示(反应条件未标出), A、B、C、D、E、W均为短周期元素,原子序数依次增大.回答下列问题:
A、B、C、D、E、W均为短周期元素,原子序数依次增大.回答下列问题: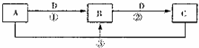
 Ⅰ
Ⅰ 2BO3(g);△H=-196.6kJ?mol-1
2BO3(g);△H=-196.6kJ?mol-1 2NGH3(g);△H=-92.4kJ/mol
2NGH3(g);△H=-92.4kJ/mol
 HCO3-+OH-
HCO3-+OH- HCO3-+OH-
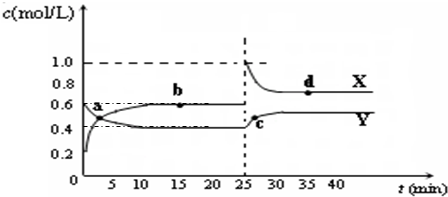
HCO3-+OH- C2D4(g);△H<0.在恒温恒容条件下,将一定量CD2和C2D4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.
C2D4(g);△H<0.在恒温恒容条件下,将一定量CD2和C2D4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.