下图为某套实验装置示意图,无法看到实验说明,加热装置已经省略.
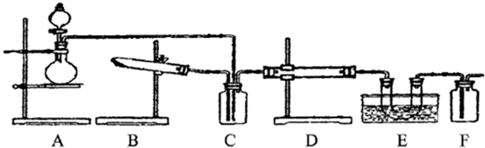
I.甲同学认为当D处盛放V
2O
5作催化剂时,此套装置可用于合成物质X,并预测E处冰水冷却的U型管中将有固体X出现.
(1)事实上此装置所附实验说明符合甲同学的推断,那么A中所发生的反应的化学方程式是
Na2SO3+H2SO4(浓)=Na2SO4+H2O+SO2↑
Na2SO3+H2SO4(浓)=Na2SO4+H2O+SO2↑
,C装置中盛放的液体药品的名称是
浓硫酸
浓硫酸
.
(2)甲同学方案中为了提高A装置产物的转化率,可以增大B装置产物的通入量,欲知A、B两装置中产物在D中的通入量,可通过观察
C中两导管口气泡的产生速率
C中两导管口气泡的产生速率
得知.
(3)本实验在设计上有无缺失之处?若有请答出改进方案
有,应在EF之间连接一个防倒吸装置
有,应在EF之间连接一个防倒吸装置
;(若无,此问可不答)
II.乙同学认为若D处盛放铂铑合金网作催化剂,则此套装置也可用于合成物质Y,并预测E处冰水冷却的U型管中将有红棕色气体生成,且越接近U型管底部颜色越浅.
(4)写出乙同学认为的D装置中发生反应的化学方程式
4NH
3+5O
24NO+6H
2O(若多写2NO+O
2=2NO
2也可以)
4NH
3+5O
24NO+6H
2O(若多写2NO+O
2=2NO
2也可以)
.
(5)对于A处,乙认为没有加热装置,请代乙阐述A中气体的产生原理
将分液漏斗中的浓氨水滴加至圆底烧瓶中的固体NaOH(或生石灰或碱石灰)中,反应放热溶液中c(OH-)增大氨水浓度增大,上述三个因素均导致氨水中的平衡:NH3+H2O?NH3?H2O?NH4++OH-向左移动致使NH3逸出
将分液漏斗中的浓氨水滴加至圆底烧瓶中的固体NaOH(或生石灰或碱石灰)中,反应放热溶液中c(OH-)增大氨水浓度增大,上述三个因素均导致氨水中的平衡:NH3+H2O?NH3?H2O?NH4++OH-向左移动致使NH3逸出
(6)若要用上述装置完成乙同学所认为的实验,且C处所起作用与合成X时所起作用基 本一致,那么C处的广口瓶应改为
U形管或干燥管
U形管或干燥管
,所装药品为
碱石灰(其他合理答案亦可)
碱石灰(其他合理答案亦可)
.



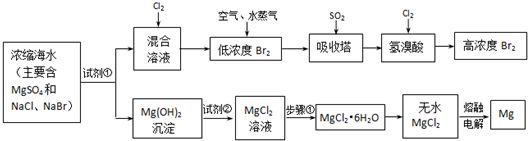
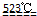 MgO+2 HCl↑+5H2O↑
MgO+2 HCl↑+5H2O↑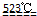 MgO+2 HCl↑+5H2O↑
MgO+2 HCl↑+5H2O↑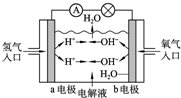 下图为氢氧燃料电池原理示意图,下列叙述正确的是( )
下图为氢氧燃料电池原理示意图,下列叙述正确的是( ) 两边基团换位的反应.
两边基团换位的反应.








