
题目列表(包括答案和解析)
某教师在上《元素周期表》复习课时,组织了一个“介绍自己”的活动:
我们班级中共有44位同学,分为8个小组(学生座位如图所示,数字表示座位号),按从左到右分别为IA、IIA……VIIA、0族,从上到下分别为第一、二……六周期。座位上的每一位同学对应一种元素,请在下列问题中符合要求的同学向大家介绍自己。
|
|
2 |
|
|
讲 台 |
|
|
3 |
|
||||
|
5 |
6 |
7 |
8 |
|
9 |
10 |
11 |
12 |
||||
|
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
|||||
|
21 |
22 |
23 |
24 |
25 |
26 |
27 |
28 |
|||||
|
29 |
30 |
31 |
32 |
33 |
34 |
35 |
36 |
|||||
|
37 |
38 |
39 |
40 |
41 |
42 |
43 |
44 |
请你一起思考并回答下列问题:
(1)第三周期IVA族的元素对应座位号是 ,原子结构示意图为 。
(2)座位号为22的元素在元素周期表中的位置是 。
(3)比较座位号为18、19对应的元素的非金属性强弱,请用离子方程式表示 。
(4)课堂中有学生提出,这样的安排会导致他们没有对应的元素,则学生对应的座位号是 。
某教师在上《元素周期表》复习课时,组织了一个“介绍自己”的活动:
我们班级中共有44位同学,分为8个小组(学生座位如图所示,数字表示座位号),按从左到右分别为IA、IIA……VIIA、0族,从上到下分别为第一、二……六周期。座位上的每一位同学对应一种元素,请在下列问题中符合要求的同学向大家介绍自己。
|
| 2 | 讲 台 | 3 |
| ||||||||||
| 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | |||||||
| 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | |||||||
| 21 | 22 | 23 | 24 | 25 | 26 | 27 | 28 | |||||||
| 29 | 30 | 31 | 32 | 33 | 34 | 35 | 36 | |||||||
| 37 | 38 | 39 | 40 | 41 | 42 | 43 | 44 | |||||||
请你一起思考并回答下列问题:
(1)第三周期IVA族的元素对应座位号是 ▲ ,原子结构示意图为
▲ 。
(2)座位号为22的元素在元素周期表中的位置是 ▲ 。
(3)比较座位号为18、19对应的元素的非金属性强弱,请用离子方程式表示
▲ 。
(4)课堂中有学生提出,这样的安排会导致他们没有对应的元素,则学生对应的座位号是 ▲ 。
Ⅰ.甲醇是一种新型的能源。
(1)合成气(组成为H2和CO)是生产甲醇的重要原料,请写出由焦炭和水在高温下制取合成气的化学方程式 。
(2)已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ·mol-1、-283.0kJ·mol-1和-726.5kJ·mol-1,则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为 ;
(3)在容积为l L的密闭容器中,由CO和H2合成甲醇。在其他条件不变的情况下,考查温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300℃);

下列说法正确的是 (填序号)
A.温度为T1时,从反应开始到平衡,生成甲醇的平均速率为v(CH3OH)= (mol·L-1·min-1)
(mol·L-1·min-1)
B.该反应在T1时的平衡常数比T2时的大
C.该反应为吸热反应
D.处于A点的反应体系从T1变到T2,达到平衡时 减小
减小
(4)在T1温度时,将1 mol CO和2mol H2充入一密闭恒容容器中,充分反应达到平衡后,若CO转化率为a,则容器内的压强与起始压强之比为 ;
(5)在直接以甲醇为燃料的电池中,电解质溶液为碱性,负极的反应式为 ;假设原电解质为NaOH,且电池工作一段时间后溶质只有Na2CO3,此时溶液中各离子浓度大小关系为
Ⅱ.已知Ksp(AgCl)=1.56×10-10 ,Ksp(AgBr)=7.7×10-13 ,Ksp(Ag2CrO4)=9×10-11。某溶液中含有C1-, Br-和CrO42-,浓度均为0.010mo1·L-1,向该溶液中逐滴加入0.010mol·L-1的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为 。
下表列出的是部分元素的原子序数,有关该表的下列说法正确的是( )
| 9 | 10 | 11 |
| 17 | 18 | 19 |
A.每一横行元素原子的电子层数都不相同
B.每一纵行元素原子的最外层电子数都不相同
C.中间的纵行元素很不容易与其他元素化合
D.左边纵行元素的金属性很强
Ⅰ.甲醇是一种新型的能源。
(1)合成气(组成为H2和CO)是生产甲醇的重要原料,请写出由焦炭和水在高温下制取合成气的化学方程式 。
(2)已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ·mol-1、-283.0kJ·mol-1和-726.5kJ·mol-1,则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为 ;
(3)在容积为l L的密闭容器中,由CO和H2合成甲醇。在其他条件不变的情况下,考查温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300℃);
下列说法正确的是 (填序号)
A.温度为T1时,从反应开始到平衡,生成甲醇的平均速率为v(CH3OH)=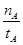 (mol·L-1·min-1) (mol·L-1·min-1) |
| B.该反应在T1时的平衡常数比T2时的大 |
| C.该反应为吸热反应 |
D.处于A点的反应体系从T1变到T2,达到平衡时 减小 减小 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com