
题目列表(包括答案和解析)

(1)正极:________________________________________________;
(2)负极:________________________________________________;
(3)电池反应:____________________________________________。
现有下列十种物质:①滴有酚酞的NaOH溶液 ②干冰 ③Na2SO4·10H2O ④纯碱 ⑤BaCl2溶液 ⑥Ca(OH)2 ⑦新制氯水 ⑧盐酸 ⑨淀粉KI试纸 ⑩Na2O
(1)上述物质中属于非电解质的是(填写序号): ▲ 。
(2)写出下列物质相互之间反应或转化的化学方程式:
a. ⑥+⑧ ▲ b. ⑦+⑨ ▲
(3)向盛有2mL①溶液的试管中逐滴加入⑦,现象为 ▲ ;试解释出现相应现象的可能原因为 ▲ ;请设计实验证明你的解释: ▲ 。
(4)将一定量的③和④形成的混合物溶于水配成100 mL溶液,量取10mL该溶液与足量的⑤反应,经过滤、洗涤、烘干后得沉淀4.30g,又把沉淀溶于足量的⑧,再经过滤、洗涤、烘干后得沉淀2.33g。试求出上述所配溶液中c(CO32-)= ▲ ;c(SO42-)= ▲ 。
 短周期主族元素A、B、C、D、E在元素周期表中的位置如下图所示:请回答下列问题:
短周期主族元素A、B、C、D、E在元素周期表中的位置如下图所示:请回答下列问题:
| ||
. |
| 1 |
| 6 |
| 1 |
| 6 |
短周期主族元素A、B、C、D、E在元素周期表中的位置如下图所示:
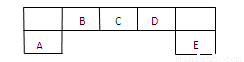
请回答下列问题:
(1)B、C、D元素电负性的大小顺序为:______>______>______(填元素符号)。
 (2)E的氢化物与其最高价氧化物的水化物的钾盐共热能发生反应,生成一种气体单质,反应的化学方程式为_______________________________________________.
(2)E的氢化物与其最高价氧化物的水化物的钾盐共热能发生反应,生成一种气体单质,反应的化学方程式为_______________________________________________.
(3)C有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2L甲气体与0.5L氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的含氧酸盐的化学式是__________.
 (4)在298K下,A、B的单质各1mol完全燃烧,分别放出热量a kJ和b kJ。又知一定条件下,A的单质能将B从它的最高价氧化物中置换出来,若此置换反应生成3molB的单质,则该反应在298K下的
(4)在298K下,A、B的单质各1mol完全燃烧,分别放出热量a kJ和b kJ。又知一定条件下,A的单质能将B从它的最高价氧化物中置换出来,若此置换反应生成3molB的单质,则该反应在298K下的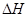 =
(注:题中所设单质均为最稳定单质)
=
(注:题中所设单质均为最稳定单质)
(5)要证明与D同主族相邻元素F的非金属性与E的非金属性的强弱,正确、合理的实验操作及现象是
(6)用A、B的单质作电极,C的最高价氧化物的水化物稀溶液作电解质溶液构成原电池,写出此原电池正极的电极反应式 。(假设C只被还原至+2价)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com