
题目列表(包括答案和解析)
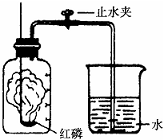 某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下:
某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下:| 点燃 |
| 点燃 |
| 1 |
| 5 |
| 1 |
| 5 |
| 1 |
| 5 |
| 1 |
| 5 |
| 7cV |
| 125a |
| 7cV |
| 125a |
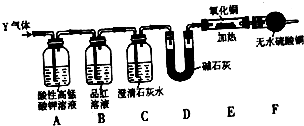
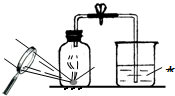
为测定Na2CO3与Na2SO3混合物中各组分的含量,取样品23.2 g按右图所示装置进行实验:(铁架台、铁夹等仪器未在图中画出)
(1)将仪器连接好以后,必须进行的第一步操作是____________________。
(2)此实验还必须用到的最重要的仪器是__________;仪器F的作用是________________________________________。
(3)已知仪器C中装有品红溶液,其作用是______________________________。
(4)实验室中备有以下常用试剂:a.浓硫酸,b.品红溶液,c.酸性高锰酸钾溶液,d.饱和碳酸氢钠溶液,e.氢氧化钠溶液,f.无水硫酸铜,g.碱石灰,h.五氧化二磷。请将下列容器中应盛放的试剂序号填入相应空格:B中__________,D中__________,E中__________。
实验过程中,当仪器A内的固体反应完全后,需打开活塞K,向A中通入大量的空气。这样做的目的是____________________。所通空气应先经过__________试剂(填上述所供试剂的序号)处理,否则可能引起Na2SO3含量的测量结果比实际值__________(填“偏高”“偏低”或“没影响”)。
(5)若仪器E在实验完成时增重4.4 g,则Na2CO3与Na2SO3的物质的量之比为__________。
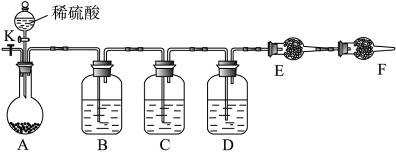
为测定Na2CO3与Na2SO3混合物中各组分的含量,取样品23.2 g,用下图所示装置进行实验(铁架台、铁夹等仪器未在图中画出):
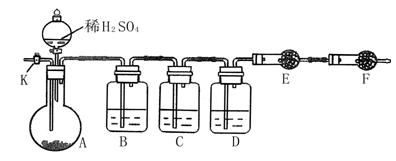
(1)将仪器连接好以后,必须进行的第一步操作是:___________________
(2)此实验还必须用到的最重要的仪器是________________ _________;
仪器F的作用是___________________________________________ _。
(3)已知仪器C中装有品红溶液,其作用是_____________________ ____。
(4)实验室中备有以下常用试剂:a.浓硫酸; b.品红溶液;c.酸性高锰酸钾溶液;d.饱和碳酸氢钠溶液;e.氢氧化钠溶液;f.无水硫酸铜;g.碱石灰;h.五氧化二磷;i.无水氯化钙。请将下列容器中应盛放的试剂序号填入相应空格:B中______,D中_________,E中__________。
(5)实验过程中,当仪器A内的固体反应完全后,需打开活塞K,向A中缓慢通入大量的空气。这样做的目的是___________ _______。所通空气应先经过___________试剂(填上述所供试剂的序号)处理,否则可能引起Na2SO3含量的测量结果比实际值_______________(填“偏高”、“偏低”或“没影响”)。
(6)若仪器E在实验完成时增重4.4 g,则Na2CO3与Na2SO3的物质的量之比为______。
为测定Na2CO3与Na2SO3混合物中各组分的含量,取样品23.2g,用下图所示装置进行实验(铁架台、铁夹等仪器未在图中画出):
(1)将仪器连接好以后,必须进行的第一步操作是:___________________
(2)此实验还必须用到的最重要的仪器是________________ _________;
仪器F的作用是___________________________________________ _。
(3)已知仪器C中装有品红溶液,其作用是_____________________ ____。
(4)实验室中备有以下常用试剂:a.浓硫酸; b.品红溶液;c.酸性高锰酸钾溶液;d.饱和碳酸氢钠溶液;e.氢氧化钠溶液;f.无水硫酸铜;g.碱石灰;h.五氧化二磷;i.无水氯化钙。请将下列容器中应盛放的试剂序号填入相应空格:B中______,D中_________,E中__________。
(5)实验过程中,当仪器A内的固体反应完全后,需打开活塞K,向A中缓慢通入大量的空气。这样做的目的是___________ _______。所通空气应先经过___________试剂(填上述所供试剂的序号)处理,否则可能引起Na2SO3含量的测量结果比实际值_______________(填“偏高”、“偏低”或“没影响”)。
(6)若仪器E在实验完成时增重4.4 g,则Na2CO3与Na2SO3的物质的量之比为______。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com