(2012?广州一模)绿矾(FeSO
4?7H
2O)的一种综合利用工艺如下:
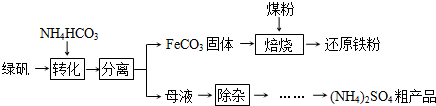
(1)绿矾与NH
4HCO
3在溶液中按物质的量之比1:2反应,有CO
2生成,反应的离子方程式为
Fe2++2HCO3-=CO2↑+FeCO3↓+H2O
Fe2++2HCO3-=CO2↑+FeCO3↓+H2O
.
(2)隔绝空气进行“焙烧”,铁元素的转化途径是FeCO
3 FeO
Fe,实际作还原剂的是CO.写出“焙烧”过程中各步反应的化学方程式
FeCO
3FeO+CO
2↑;C+CO
22CO;CO+FeO
Fe+CO
2FeCO
3FeO+CO
2↑;C+CO
22CO;CO+FeO
Fe+CO
2.
(3)“除杂”步骤为:向母液中通入含臭氧的空气、调节pH、过滤,除去的杂质离子是
Fe2+
Fe2+
.
(4)母液“除杂”后,欲得到(NH
4)
2SO
4粗产品,操作步骤依次为真空蒸发浓缩、冷却结晶、
过滤
过滤
.浓缩时若温度过高,产品中将混有NH
4HSO
4,运用化学平衡移动原理解释其原因
NH4++H2O?NH3?H2O+H+,温度过高一水合氨分解氨气挥发,平衡正向进行,酸性增强生成硫酸氢铵
NH4++H2O?NH3?H2O+H+,温度过高一水合氨分解氨气挥发,平衡正向进行,酸性增强生成硫酸氢铵
.
(5)绿矾的另一种综合利用方法是:绿矾脱水后在有氧条件下焙烧,FeSO
4转化为Fe
2O
3和硫的氧化物.分析下表实验数据,为了提高SO
3的含量,可采取的措施是
增大空气通入量
增大空气通入量
.
| 空气通入量/L?s-1 |
温度/℃ |
SO2含量/% |
SO3含量/% |
| 0.02 |
850 |
45.4 |
54.6 |
| 0.06 |
850 |
30.5 |
69.5 |
| 0.10 |
850 |
11.1 |
88.9 |
| 0.10 |
810 |
11.1 |
88.9 |
| 0.10 |
890 |
11.2 |
88.8 |


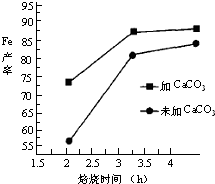 利用生产钛白的副产品绿矾(FeSO4?7H2O)制备还原铁粉的步骤如下:将绿矾溶于稀硫酸溶液,向其中滴加(NH4)2CO3溶液,得到FeCO3?nH2O沉淀,静置,过滤,洗涤,干燥,再将FeCO3与煤粉一起焙烧,最终制得还原铁粉.涉及的主要反应有:
利用生产钛白的副产品绿矾(FeSO4?7H2O)制备还原铁粉的步骤如下:将绿矾溶于稀硫酸溶液,向其中滴加(NH4)2CO3溶液,得到FeCO3?nH2O沉淀,静置,过滤,洗涤,干燥,再将FeCO3与煤粉一起焙烧,最终制得还原铁粉.涉及的主要反应有:
