
题目列表(包括答案和解析)
| A.需要加热才能进行的反应一定是吸热反应,放热反应不需要加热 |
| B.一定条件下进行的化学反应,只能将化学能转化成光能或热能 |
| C.电解质导电的过程实际是一个电解的过程,此过程中电能转化成化学能 |
| D.电镀是利用原电池的原理,在易被腐蚀的金属表面包上一层不易被腐蚀的金属薄片 |
A.焰色反应是化学反应
B.焰色反应是物理变化
C.焰色反应既可以在化学变化中表现出来,也可以在物理变化中表现出来
D.焰色反应能够鉴别所有的金属或金属离子
废弃物的综合利用既有利于节约资源,又有利于保护环境。实验室利用废旧电池的铜帽(Cu、Zn总含量约为99%)回收Cu并制备ZnO的部分实验过程如下:
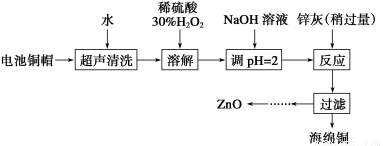
(1)①铜帽溶解时加入H2O2的目的是________________________________________
(用化学方程式表示)。
②铜帽溶解完全后,需将溶液中过量的H2O2除去。除去H2O2的简便方法是_______________________________________________________________。
(2)为确定加入锌灰(主要成分为Zn、ZnO,杂质为铁及其氧化物)的量,实验中需测定除去H2O2后溶液中Cu2+的含量。实验操作为:准确量取一定体积的含有Cu2+的溶液于带塞锥形瓶中,加适量水稀释,调节溶液pH=3~4,加入过量的KI,用Na2S2O3标准溶液滴定至终点。上述过程中发生反应的离子方程式如下:
2Cu2++4I-=2CuI(白色)↓+I2
2S2O32—+I2=2I-+S4O62—
①滴定选用的指示剂为__________,滴定终点观察到的现象为__________________。
②若滴定前溶液中的H2O2没有除尽,所测定的Cu2+含量将会________(填“偏高”、“偏低”或“不变”)。
(3)已知pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-。下表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)。
| 开始沉淀的pH | 沉淀完全的pH |
Fe3+ | 1.1 | 3.2 |
Fe2+ | 5.8 | 8.8 |
Zn2+ | 5.9 | 8.9 |
、实验中可选用的试剂:30% H2O2、1.0 mol·L-1 HNO3、1.0 mol·L-1 NaOH。
由除去铜的滤液制备ZnO的实验步骤依次为
①______________________________________;
②________________________________________;
③过滤;
④_________________________________________;
⑤过滤、洗涤、干燥;
⑥900 ℃煅烧。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com