
题目列表(包括答案和解析)
某蓄电池充放电的反应如下:Fe +
NiO2 + 2H2O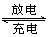 Fe(OH)2 +Ni(OH)2 下列推断中正确的是
Fe(OH)2 +Ni(OH)2 下列推断中正确的是
A.放电时,Fe是正极
B.充电时阴极电极反应式为:Fe ( OH )2 + 2e-=Fe + 2OH-
C.充电时,Ni元素被还原
D.放电时溶液中OH-移向正极
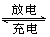 Fe(OH)2 +Ni(OH)2 下列推断中正确的是
Fe(OH)2 +Ni(OH)2 下列推断中正确的是| A.放电时,Fe是正极 |
| B.充电时阴极电极反应式为:Fe ( OH )2 + 2e-=Fe + 2OH- |
| C.充电时,Ni元素被还原 |
| D.放电时溶液中OH-移向正极 |
某蓄电池充放电的反应如下:Fe + NiO2 + 2H2O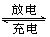 Fe(OH)2 +Ni(OH)2 下列推断中正确的是
Fe(OH)2 +Ni(OH)2 下列推断中正确的是
| A.放电时,Fe是正极 |
| B.充电时阴极电极反应式为:Fe ( OH )2 + 2e-=Fe + 2OH- |
| C.充电时,Ni元素被还原 |
| D.放电时溶液中OH-移向正极 |
蓄电池在放电时起原电池作用,在充电时起电解池的作用.下式是爱迪生蓄电池分别在充电和放电时发生的反应:
Fe+NiO2+2H2O![]() Fe(OH)2+Ni(OH)2,下列有关对爱迪生蓄电池的推断错误的是
Fe(OH)2+Ni(OH)2,下列有关对爱迪生蓄电池的推断错误的是
[ ]
A.放电时铁作负极,NiO2作正极
B.充电时阴极的电极反应式为:Fe(OH)2+2e-=Fe+2OH-
C.放电时电解质溶液中的阴离子向正极方向移动
D.蓄电池的电极必需浸入某种碱性电解质溶液中
(1)0.1mol/L Na2CO3溶液呈 (填“酸性”、“碱性”或“中性”),其原因是 (用离子方程式表示)
(2)氢氧燃料电池是利用氢能的一种重要方式。请写出氢氧燃料电池(电解质溶液为KOH溶液)的负极的电极反应式 ;
(3)某温度下的水溶液中,c(H+)=10-xmol/L,c(OH-)=10-y mol/L。x与y的关系如图所示,该温度下水的离子积为 ;该温度下0.01 mol/L NaOH溶液的pH为 。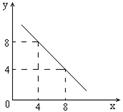
(4)如图装置,已知两电极上发生的电极反应分别为:
a极:Cu2++2e-= Cu b极:Fe-2e-= Fe2+
该装置中原电解质溶液一定含有 ;(填序号)
| A.Cu2+ | B.Na+ | C.Fe2+ | D.Ag+ |

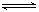 Ba2+ (aq)+ SO42-(aq) 25℃时,BaSO4的Ksp=1.1×l0—10,在0.1 mol·L一1硫酸溶液中,钡离子的浓度最大可达到 mol·L一1。
Ba2+ (aq)+ SO42-(aq) 25℃时,BaSO4的Ksp=1.1×l0—10,在0.1 mol·L一1硫酸溶液中,钡离子的浓度最大可达到 mol·L一1。湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com