
题目列表(包括答案和解析)
将1 mol![]() 和3 mol
和3 mol![]() 充入一密闭容器中,使其在一定条件下达到平衡:
充入一密闭容器中,使其在一定条件下达到平衡:![]()
![]()
![]() ,下列哪一状态一定是平衡状态( )
,下列哪一状态一定是平衡状态( )
(1)混合气体的体积等于最初一半的状态;
(2)氮气、氢气和氨的总物质的量不随时间延长而改变的状态;
(3)氮气、氢气和氨的总质量不随时间延长而改变的状态;
(4)单位时间有1 mol氨消耗的同时,就有0.5 mol氮气生成的状态;
(5)单位时间有1 mol氨消耗的同时,有0.5 mol氮气和1.5 mol氢气生成氨的状态;
(6)氮气和氢气体积百分含量之比不随时间延长而改变的状态;
(7)氮气、氢气和氨三者的质量之比不随时间延长而改变的状态;
(8)正、逆反应同时进行的状态;
(9)氢气减少的速率等于氨增加的速率的状态;
(10)氮气、氢气和氨三者浓度相等的状态;
(11)外界条件的改变不影响组成分质量分数的状态;
(12)氨的生成速率与其消耗速率相等的状态.
(1)混合气体的体积等于最初一半的状态;
(2)氮气、氢气和氨的总物质的量不随时间延长而改变的状态;
(3)氮气、氢气和氨的总质量不随时间延长而改变的状态;
(4)单位时间有1 mol氨消耗的同时,就有0.5 mol氮气生成的状态;
(5)单位时间有1 mol氨消耗的同时,有0.5 mol氮气和1.5 mol氢气生成氨的状态;
(6)氮气和氢气体积百分含量之比不随时间延长而改变的状态;
(7)氮气、氢气和氨三者的质量之比不随时间延长而改变的状态;
(8)正、逆反应同时进行的状态;
(9)氢气减少的速率等于氨增加的速率的状态;
(10)氮气、氢气和氨三者浓度相等的状态;
(11)外界条件的改变不影响组成分质量分数的状态;
(12)氨的生成速率与其消耗速率相等的状态.
| 5 |
| 7 |
| 5 |
| 7 |
(11分)以CO2为碳源制取低碳有机物成为国际研究焦点,下面为CO2加氢制取低碳醇的热力学数据:
反应I:
CO2(g)+3H2(g) CH3OH(g)+H2O(g)
△H = —49.0 kJ·mol-1
CH3OH(g)+H2O(g)
△H = —49.0 kJ·mol-1
反应II:2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(g)
△H = —173.6 kJ·mol-1
CH3CH2OH(g)+3H2O(g)
△H = —173.6 kJ·mol-1
(1)写出由CH3CH2OH +_____ 2CH3OH的热化学方程式为:__________________。
2CH3OH的热化学方程式为:__________________。
(2)在一定条件下,对于反应I:在体积恒定的密闭容器中,达到平衡的标志是__ (填字母)
a.CO2和CH3OH 浓度相等 b.H2O的百分含量保持不变
c.H2的平均反应速率为0 d.v正(CO2)=3v逆(H2)
e.混合气体的密度不再发生改变
f. 混合气体的平均相对分子质量不再发生改变
如果平衡常数K值变大,该反应 (填字母)
a.一定向正反应方向移动 b.在平衡移动时正反应速率先增大后减小
c.一定向逆反应方向移动 d.在平衡移动时逆反应速率先减小后增大
其他条件恒定,如果想提高CO2的反应速率,可以采取的反应条件是 (填字母) ,
达到平衡后,想提高H2转化率的是_______________(填字母)
a、降低温度 b、补充H2 c、移去甲醇 d、加入催化剂
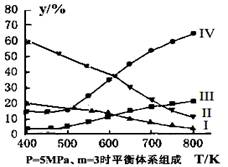
(3)在密闭容器中,对于反应II中,研究员以生产乙醇为研究对象,在5MPa、m= n(H2)/n(CO2)=3时,测得不同温度下平衡体系中各种物质的体积分数(y%)如图所示,则表示CH3CH2OH体积分数曲线的是 ;表示CO2的体积分数曲线的是 。
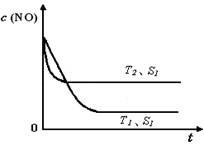
(4)当质量一定时,增大固体催化剂的表面积可提高化学反应速率。上图是反应:2NO(g)
+ 2CO(g)
 2CO2(g)+ N2(g) 中NO的浓度随温度(T)、催化剂表面积(S)和时间(t)的变化曲线, 若催化剂的表面积S1>S2 ,在上图中画出NO的浓度在T1、S2 条件下达到平衡过程中的变化曲线,并注明条件。
2CO2(g)+ N2(g) 中NO的浓度随温度(T)、催化剂表面积(S)和时间(t)的变化曲线, 若催化剂的表面积S1>S2 ,在上图中画出NO的浓度在T1、S2 条件下达到平衡过程中的变化曲线,并注明条件。
23.(10分)(1)一种气态烷烃和一种气态烯烃的混合物10g,其密度是相同条件下氢气密度的12.5倍,当此混合气体通过足量溴水时,溴水质量增重8.4 g,则这两种烃分别为 , ;体积比
(2)0.1mol某烃完全燃烧,生成10.8g H2O和11.2LCO2(标准状况下)。则该烃的分子式: ;在其同分异构体中,一氯代物只有一种的结构简式是:
(3) 往一容积为10 L的密闭容器中充入2 mol N2、4 mol H2进行合成氨反应N2+3H2 2NH3。5 min后达到平衡,该合成反应5 min内的速率v(NH3)= 0.02 mol/(L·min)。试求平衡时,容器中N2转化率是
。
2NH3。5 min后达到平衡,该合成反应5 min内的速率v(NH3)= 0.02 mol/(L·min)。试求平衡时,容器中N2转化率是
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com