
题目列表(包括答案和解析)
 7N2(g)+12H2O(g)也可处理NO2。则化学平衡常数表达式K=______;当转移1.2mol电子时,消耗的NO2在标准状况下是_______L。
7N2(g)+12H2O(g)也可处理NO2。则化学平衡常数表达式K=______;当转移1.2mol电子时,消耗的NO2在标准状况下是_______L。 
 CO2+H2(g) 反应过程中测定的部分数据见下表(表中t1>t2)
CO2+H2(g) 反应过程中测定的部分数据见下表(表中t1>t2) 

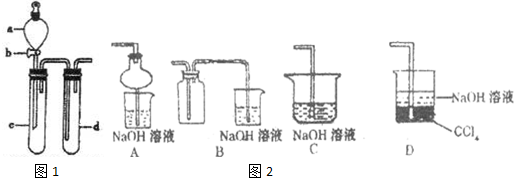
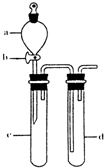 SO2是一种重要的化工原料,也是引起酸雨污染的重要来源.
SO2是一种重要的化工原料,也是引起酸雨污染的重要来源.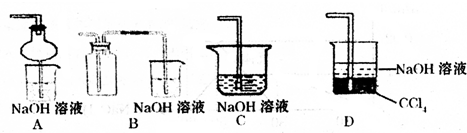
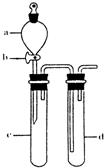 SO2是一种重要的化工原料,也是引起酸雨污染的重要来源.
SO2是一种重要的化工原料,也是引起酸雨污染的重要来源.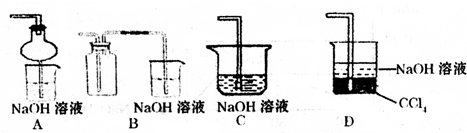
可持续发展是全球经济发展的共同课题,珍惜地球,保护环境已成为我国的基本国策.汽车尾气(含烃类、CO、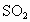 、NO等物质)是城市空气的污染源.治理方法之一是在汽车排气管上装一个“催化转换器”(用铂、钯合金作催化剂),它的特点是使CO与NO反应,生成两种可参与大气生态环境循环的无毒气体,并促使烃类充分燃烧及
、NO等物质)是城市空气的污染源.治理方法之一是在汽车排气管上装一个“催化转换器”(用铂、钯合金作催化剂),它的特点是使CO与NO反应,生成两种可参与大气生态环境循环的无毒气体,并促使烃类充分燃烧及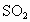 的催化氧化.
的催化氧化.
(1)写出CO与NO在催化剂作用下的反应方程式:__________________.
(2)“催化剂转换器”的缺点是在一定程度上提高了空气的酸度,其原因是___________________________________________________________.
(3)控制城市空气污染源的方法可行的有
[ ]
(4)汽车尾气经“催化转换器”处理后的大量气体使地球的温室效应增强,下列叙述中不正确的应该是
[ ]
A.如果没有地球的自然温室效应,大多数的生命都将不存在
D.全球工业发展造成温室效应的恶化,导致全球变暖
C.限制发展中国家的工业气体排放,可以使大气中温室气体浓度趋于稳定水平
D.森林大幅度地吸收二氧化碳,可缓解全球温室效应的危机
(5)现代科学技术的迅速发展和广泛应用,带来了经济增长,却使全球面临资源枯竭、环境污染、生态污染和生态失衡等一系列危机,这说明_____________________________________________________________.
[ ]
A.任何事物都是一分为二的
B.科学技术的发展是产生危机的根源
C.旧的矛盾解决了,又会产生新的矛盾
D.规律是客观的,违背规律是要遭到惩罚的
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com