
题目列表(包括答案和解析)
| 元素编号 | 元素性质或原子结构 |
| A | A原子所处的周期数、族序数、原子序数均相等 |
| B | 核外电子有6种不同运动状态 |
| C | 最简单氢化物的水溶液呈碱性 |
| D | 基态原子的S轨道电子数等于P轨道电子数 |
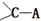 所得ABCD的结构式为
所得ABCD的结构式为纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域。单位质量的A和B单质燃烧时均放出大量热,可用作燃料。已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
| 电离能(kJ/mol) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
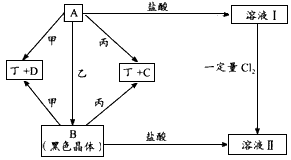
(1)某同学根据上述信息,推断B的核外电子排布如右图所示 ,
,
该同学所画的电子排布图违背了 。
(2)根据价层电子对互斥理论,预测A和氯元素形成的简单分子空间构型为 。
(3)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料。已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145~140pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确 (填是、否),并阐述理由 。

 (4)科学家把C60和钾掺杂在一起制造了一种富勒烯化合物, 其晶胞如图所示,该物质在低温时是一种超导体。写出基态钾原子的价电子排布式 ,该物质的K原子和C60分子的个数比为 。
(4)科学家把C60和钾掺杂在一起制造了一种富勒烯化合物, 其晶胞如图所示,该物质在低温时是一种超导体。写出基态钾原子的价电子排布式 ,该物质的K原子和C60分子的个数比为 。
(5)继C60后,科学家又合成了Si60、N60,C、Si、N原子电负性由大到小的顺序是 。Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则Si60分子中π键的数目为 。
(6) 晶体硼的基本结构单元是由硼原子组成的正二十面体的原子晶体。其中含有20个等边三角形和一定数目的顶角,每个顶角各有一个原子,试观察图形回答:这个基本结构单元由_____个硼原子组成,共含有________个B-B键。
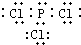
| 3 |
| 2 |
| 3 |
| 2 |

请按要求回答下列问题:
(1)画出E的离子结构示意图____________,写出由A和C组成的含有非极性键的化合物的电子式:____________。
(2)由上述元素组成的化合物中属于极性键构成的非极性分子的是____________(只要求写出两种,用化学式表示)。
(3)由C与E形成的化合物高温时与B反应生成两种化合物,请写出该反应的化学方程式:________________________。
(4)写出上述元素形成的化合物中一种可溶性的正盐与另一种强酸反应的离子方程式:________________________。
(5)上述元素形成的化合物中通常能污染空气的是________________________(至少写出两种)。某一种可污染空气的化合物与强氧化剂单质常温下反应生成两种化合物,该反应的化学方程式为:_____________________________________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com