
题目列表(包括答案和解析)
下列说法正确的是( )
A.HCl溶液中无OH-
B.NaOH溶液中无H+
C.NaCl溶液中既无H+,也无OH-
D.常温下,任何物质的水溶液中都有H+和OH-,且c(H+)·c(OH-)=10-14
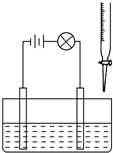 在烧杯里加入20mL 0.1mol?L-1的Ba(OH)2溶液,再滴几滴酚酞试液,然后用滴定管向烧杯中滴加等物质的量浓度的NaHSO4溶液.实验装置如图(夹持仪器已去掉):
在烧杯里加入20mL 0.1mol?L-1的Ba(OH)2溶液,再滴几滴酚酞试液,然后用滴定管向烧杯中滴加等物质的量浓度的NaHSO4溶液.实验装置如图(夹持仪器已去掉):+ 4 |
+ 4 |
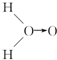 (式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂)
(式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂)

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com