
(2013?绍兴二模)苯甲酸乙酯(C
9H
10O
2)(Mr=150)(密度1.05g?cm
-3)稍有水果气味,用于配制香水香精和人造精油;也大量用于食品中,也可用作有机合成中间体、溶剂如纤维素酯、纤维素醚、树脂等.可能用到的数据:
| 沸点(℃,1atm) |
| 苯甲酸 |
苯甲酸乙酯 |
石油醚 |
水 |
乙醇 |
环己烷 |
共沸物(环已烷-水-乙醇) |
| 249 |
212.6 |
40-80 |
100 |
78.3 |
80.75 |
62.6 |
其制备原理如下:

制备过程:
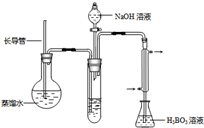
(1)制备粗产品:如图所示的装置中,于50mL圆底烧瓶中加入8.0g苯甲酸(固体)(Mr=122)、20mL乙醇(Mr=46)、15mL环己烷、3mL浓硫酸,摇匀,加沸石.在分水器上加水至c处,接通冷凝水,水浴回流约2h,反应基本完成.记录体积,继续蒸出多余的环己烷和乙醇(从分水器中放出).
(2)粗产品的纯化:加水30mL,分批加入固体NaHCO
3.分液,水层用20mL石油醚分两次萃取.合并有机层,用无水硫酸镁干燥.回收石油醚,加热精馏,收集210-213℃馏分.
(1)仪器d的名称
冷凝管、水冷凝管或球形冷凝管
冷凝管、水冷凝管或球形冷凝管
,水流方向为
a
a
进
b
b
出.
(2)该反应水浴控制的温度为
略高于62.6℃
略高于62.6℃
.
(3)该反应加过量乙醇的目的为
乙醇相对廉价,增大反应物浓度,使平衡向正反应方向移动,提高苯甲酸的转化率,提高产率;形成恒沸物需要添加乙醇
乙醇相对廉价,增大反应物浓度,使平衡向正反应方向移动,提高苯甲酸的转化率,提高产率;形成恒沸物需要添加乙醇
.
(4)分水器的作用
分离产生的水,使平衡向正反应方向移动,提高转化率
分离产生的水,使平衡向正反应方向移动,提高转化率
,分水器的检漏方法
关闭活塞,在分水器中加适量的水,观察是否漏水,若不漏水,旋转活塞180°,若仍不漏水,说明分水器不漏水
关闭活塞,在分水器中加适量的水,观察是否漏水,若不漏水,旋转活塞180°,若仍不漏水,说明分水器不漏水
.如何利用实验现象判断反应已基本完成
加热回流至分水器中水位不再上升
加热回流至分水器中水位不再上升
.
(5)固体碳酸氢钠的作用
中和硫酸和未反应的苯甲酸
中和硫酸和未反应的苯甲酸
,加至
不再有气泡产生或pH=7
不再有气泡产生或pH=7
为止.
(6)经精馏得210-213℃馏分7.0mL,则该反应的产率为
73.7%
73.7%
.

 ④取下锥形瓶,滴加指示剂,用0.1000mol?L-1盐酸标准液滴定;
④取下锥形瓶,滴加指示剂,用0.1000mol?L-1盐酸标准液滴定;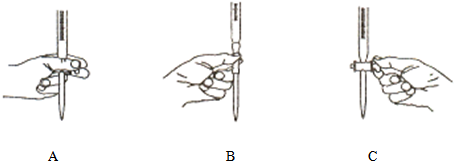
 (2013?绍兴二模)苯甲酸乙酯(C9H10O2)(Mr=150)(密度1.05g?cm-3)稍有水果气味,用于配制香水香精和人造精油;也大量用于食品中,也可用作有机合成中间体、溶剂如纤维素酯、纤维素醚、树脂等.可能用到的数据:
(2013?绍兴二模)苯甲酸乙酯(C9H10O2)(Mr=150)(密度1.05g?cm-3)稍有水果气味,用于配制香水香精和人造精油;也大量用于食品中,也可用作有机合成中间体、溶剂如纤维素酯、纤维素醚、树脂等.可能用到的数据:
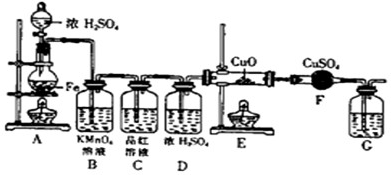
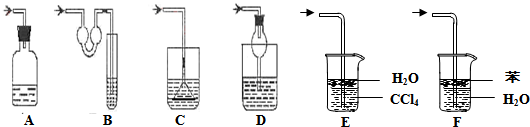
 如图所示,用排饱和食盐水法先后收集20ml CH4和80ml Cl2,放在光亮的地方(注意:不要放在日光直射的地方,以免引起爆炸),等待片刻,观察发生的现象.回答下列问题:
如图所示,用排饱和食盐水法先后收集20ml CH4和80ml Cl2,放在光亮的地方(注意:不要放在日光直射的地方,以免引起爆炸),等待片刻,观察发生的现象.回答下列问题: