
题目列表(包括答案和解析)
| 营养素 | 每份含量 |
| 油脂 | 23.5g |
| 糖类 | 104.7g |
| 维生素 | 3.5g |
| 钠 | 814mg |
| 钙 | 130mg |
| 水 | 小于210g |

碳、氢、氟、氮、硅等非金属元素与人类的生产生活息息相关。回答下列问题。
(1)写出硅原子的电子排布式________。C、Si、N的电负性由大到小的顺序是________。
(2)氟化氢水溶液中存在的氢键有________种。
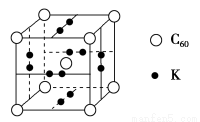
(3)科学家把C60和K掺杂在一起制造了一种富勒烯与钾的化合物,该物质在低温时是一种超导体,其晶胞如图所示,该物质中K原子和C60分子的个数比为________。
(4)继C60后,科学家又合成了Si60、N60。请解释如下现象:熔点Si60>N60>C60,而破坏分子所需要的能量N60>C60>Si60,其原因是________________________。

[物质结构与性质]
碳氢氟氮硅等非金属元素与人类的生产生活息息相关.回答下列问题:
(1)写出硅原子的电子排布式________.C、Si、N的电负性由大到小的顺序是________.
(2)氟化氢水溶液中存在氢键有________种.
(3)科学家把C60和K掺杂在一起制造了一种富勒烯与钾的化合物,该物质在低温时是一种超导体,其晶胞如图所示,该物质中K原子和C60分子的个数比为________.

(4)继C60后,科学家又合成了Si60、N60.请解释如下现象:熔点:
Si60>N60>C60,而破坏分子所需要的能量:
N60>C60>Si60,其原因是:________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com