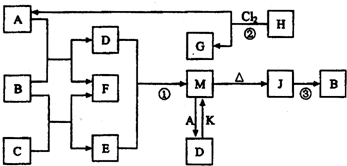
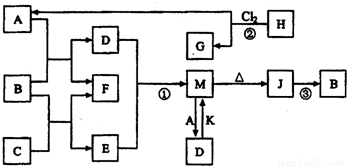
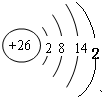
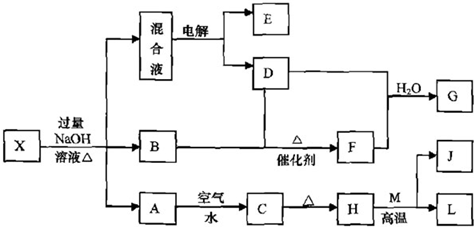
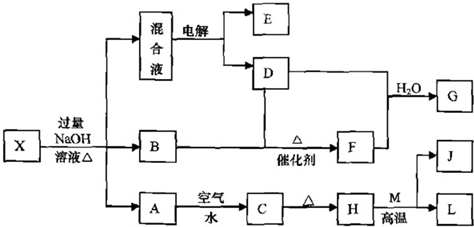
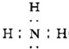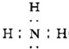有一化合物X,其水溶液为浅绿色,可发生如下的转化关系(部分反应物、生成物已略).其中,B、D、E、F均为无色气体,M、L为日常生活中常见的两种金属单质,其中L的组成元素的原子序数是M的组成元素的原子序数的2倍,H和M反应可放出大量的热.在混合液中加入BaCl
2溶液可生成不溶于稀盐酸的白色沉淀.
请回答下列问题:
(1)化合物B的电子式为
,H和M反应的一个应用
焊接钢轨
焊接钢轨
.
(2)若L的组成元素的原子最外层有2个电子,写出L的组成元素的原子结构示意图
.
(3)物质X的水溶液中各离子浓度的大小顺序是
c(SO42-)>c(NH4+)>c(Fe2+)>c(H+)>c(OH-)
c(SO42-)>c(NH4+)>c(Fe2+)>c(H+)>c(OH-)
.
(4)简述A到C的实验现象
白色沉淀迅速变成灰绿色,最后变成红褐色
白色沉淀迅速变成灰绿色,最后变成红褐色
.
(5)①写出D与F反应生成G的化学方程式
4NO+3O2+2H2O═4HNO3
4NO+3O2+2H2O═4HNO3
.
②写出X与过量的NaOH溶液反应的离子方程式
2NH4++Fe2++4OH-═Fe(OH)2+2NH3+2H2O
2NH4++Fe2++4OH-═Fe(OH)2+2NH3+2H2O
.
(6)已知a g E气体在D中完全燃烧生成稳定的化合物时,放出bKJ的热量,写出E燃烧热的热化学方程式
H
2(g)+2Fe
2O
3+8SO
2O
2(g)═H
2O(1)△H=
-kJ/mol
H
2(g)+2Fe
2O
3+8SO
2O
2(g)═H
2O(1)△H=
-kJ/mol
.

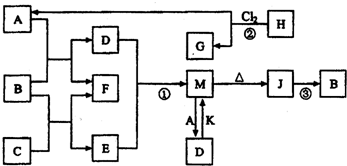 (1)C中存在的化学键类型为______;G的电子式为______.
(1)C中存在的化学键类型为______;G的电子式为______.