
题目列表(包括答案和解析)
(12分)
用下列几个实验,可快速制取实验室所需的少量气体,并进行相关性质实验。(实验装置如右图所示)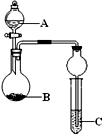
(1)若B中是生石灰,C中盛有AlCl3溶液,将A中液体逐滴加入B内,实验
中观察到C溶液中出现白色沉淀。则A中液体的是 (填名称)
C中发生反应的离子方程式为 。
(2)若要制O2,B为黑色固体,A中的试剂是 (填化学式),C中盛
有FeCl2和KSCN的混合液,旋开分液漏斗的开关后,发现C中溶液变为
血红色,写出C 中发生氧化还原反应的离子方程式 。
(3)已知氧化性强弱:KMnO4>Cl2>KIO3>I2。若A中装有浓盐酸,B中装有固体KMnO4,C中盛有KI淀粉溶液,C中的现象是 ,继续反应一段时间后,发现C中溶液的颜色褪去,这是因为
(12分)
用下列几个实验,可快速制取实验室所需的少量气体,并进行相关性质实验。(实验装置如图所示)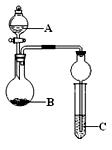
(1)若B中是生石灰,C中盛有AlCl3溶液,将A中液体逐滴加入B内,实验中观察到C溶液中出现白色沉淀。则A中液体的是 (填名称),C中发生反应的离子方程式为 。
(2)若要制O2,B为黑色固体,A中的试剂是 (填化学式),C中盛有FeCl2和KSCN的混合液,旋开分液漏斗的开关后,发现C中溶液变为血红色,写出C 中发生氧化还原反应的离子方程式 。
(3)已知氧化性强弱:KMnO4>Cl2>KIO3>I2。若A中装有浓盐酸,B中装有固体KMnO4,C中盛有KI淀粉溶液,C中的现象是 ,继续反应一段时间后,发现C中溶液的颜色褪去,这是因为 。
(12分)
用下列几个实验,可快速制取实验室所需的少量气体,并进行相关性质实验。(实验装置如右图所示)
(1)若B中是生石灰,C中盛有AlCl3溶液,将A中液体逐滴加入B内,实验
中观察到C溶液中出现白色沉淀。则A中液体的是 (填名称)
C中发生反应的离子方程式为 。
(2)若要制O2,B为黑色固体,A中的试剂是 (填化学式),C中盛
有FeCl2和KSCN的混合液,旋开分液漏斗的开关后,发现C中溶液变为
血红色,写出C 中发生氧化还原反应的离子方程式 。
(3)已知氧化性强弱:KMnO4>Cl2>KIO3>I2。若A中装有浓盐酸,B中装有固体KMnO4,C中盛有KI淀粉溶液,C中的现象是 ,继续反应一段时间后,发现C中溶液的颜色褪去,这是因为
(16分)运用相关原理,回答下列各小 题:
题:
Ⅰ.已知NaHSO4在水中的电离方程式为NaHSO4=Na++ H++ SO4 2-。
2-。
(1)在NaHSO4溶液中c(H+) c(OH-)+ c(SO42-)(填“>”、“=”或“< ”
” 下同);用硫酸氢钠与氢氧化钡溶液制取硫酸钡,若溶液中SO42-完全沉淀,则反应后溶液的pH 7。
下同);用硫酸氢钠与氢氧化钡溶液制取硫酸钡,若溶液中SO42-完全沉淀,则反应后溶液的pH 7。
(2)将 20mLpH=2的NaHSO4溶液逐滴加入到20mL 0.1 mol·L-1Na2CO3溶液中,溶液中发生反应的离子方程式为: ;向此反应后的溶液中滴加
20mLpH=2的NaHSO4溶液逐滴加入到20mL 0.1 mol·L-1Na2CO3溶液中,溶液中发生反应的离子方程式为: ;向此反应后的溶液中滴加
0.001 mol·L-1BaCl2溶液,首先析出的沉淀是 。[KSP(BaSO4)=1.1×10-10mol2·L-2;KSP(BaCO3)=5.1×10-9mol2·L-2]
Ⅱ.已知:在25时 H2O H++OH- KW=10-14
H++OH- KW=10-14
CH3COOH
 H++CH3COO--> Ka=1.8×10-5
H++CH3COO--> Ka=1.8×10-5
(3)醋酸钠水解的平衡常数Kh的表达式为 。当升高温度时,Kh将 (填“增大”“减小”“不变”);
(4)0.5mol·L-1醋酸钠溶液pH为m,其水解的程度(已水解的醋酸钠与原有醋酸钠的比值)
 为a;1mol·L-1醋酸钠溶液pH为n,水解的程度为b,则m与n的关系为 ,a与b的关系为 (填“大于”“小于”“等于”);
为a;1mol·L-1醋酸钠溶液pH为n,水解的程度为b,则m与n的关系为 ,a与b的关系为 (填“大于”“小于”“等于”);
(5)0.9mol·L-1醋酸钠溶液中[OH-]= mol·L-1
在某溶液中含Mg2+、Cd2+、Zn2+三种离子的浓度均为0.01mol·L-1。向其中加入固体醋酸钠,使其浓度为0.9mol·L-1,以上三种金属离子中 能生成沉淀,原因是 。
(KSP[Mg(OH)2]=1.8×10-11、KSP[Zn(OH)2]=1.2×10-17、
KSP[Cd(OH)2]=2.5×10-14、 =2.2)
=2.2)
(12分)
用下列几个实验,可快速制取实验室所需的少量气体,并进行相关性质实验。(实验装置如右图所示)
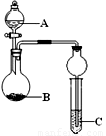
(1)若B中是生石灰,C中盛有AlCl3溶液,将A中液体逐滴加入B内,实验
中观察到C溶液中出现白色沉淀。则A中液体的是 (填名称)
C中发生反应的离子方程式为 。
(2)若要制O2,B为黑色固体,A中的试剂是 (填化学式),C中盛
有FeCl2和KSCN的混合液,旋开分液漏斗的开关后,发现C中溶液变为
血红色,写出C 中发生氧化还原反应的离子方程式 。
(3)已知氧化性强弱:KMnO4>Cl2>KIO3>I2。若A中装有浓盐酸,B中装有固体KMnO4,C中盛有KI淀粉溶液,C中的现象是 ,继续反应一段时间后,发现C中溶液的颜色褪去,这是因为
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com