
题目列表(包括答案和解析)
|
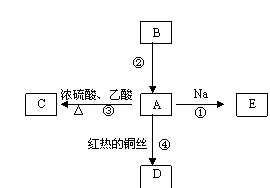
| |
(2)写出下列反应的化学方程式
反应①:
反应④:
(3)实验室利用反应③制取C,常用右图装置:
①a试管中的主要化学反应的化学方程式为
| |
![]() ②在实验中球形干燥管除起冷凝作用外,另一个重要作用 是 。
②在实验中球形干燥管除起冷凝作用外,另一个重要作用 是 。
③试管b中观察到的现象是 。
(11分)硫酸铜是一种应用极其广泛的化工原料;以下是某工厂用含铁废铜为原料生产胆矾(CuSO4·5H2 O)和副产物 石膏(CaSO4·2H2O)的生产流程示意图:
石膏(CaSO4·2H2O)的生产流程示意图: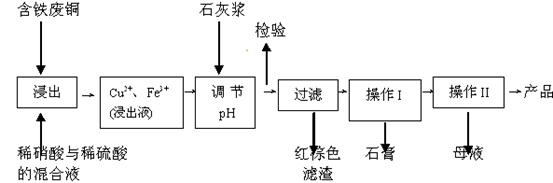
胆矾和石膏在不同温度下的溶解度(g/100g水)见下表。
温度( C) C) | 20 | 40 | 60 | 80 | 100 |
| 石膏 | 0.32[来源:Z|xx|k.Com] | 0.26 | 0.15 | 0.11 | 0.07 |
| 胆矾 | 32 | 44.6 | 61.8 | 83.8[来源:学*科*网] | 114 |
 C左右;
C左右;硫酸是强酸,中学阶段将硫酸在水溶液中看作完全电离。但事实是,硫酸在水中的第一步电离是完全的,第二步电离并不完全,其电离情况为:H2SO4=H++HSO4-,HSO4- H++SO42-.
H++SO42-.
请据此回答下列有关问题:
(1)Na2SO4溶液呈 (填“弱酸性”、“中性”或“弱碱性”),原因是: (用离子方程式表示)
(2)写出H2SO4溶液与BaCl2溶液反应的离子方程式: ;
(3)在0.1 mol·L-1的Na2SO4溶液中,下列粒子浓度关系式正确的是 。(填编号)
| A.c(SO42-)+c(HSO4-)=0.1 mol·L-1 | B.c(SO42-)+c(HSO4-)=2 c(Na+) |
| C.c(OH-)=c(H+)+c(HSO4-) | D.c(Na+)+c(H+)=c(OH-)+c(HSO4-) |


湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com