
题目列表(包括答案和解析)
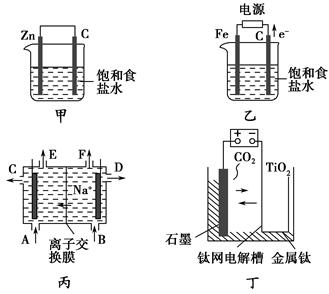
甲、乙的实验装置如图所示,丙、丁分别是氯碱工业生产示意图和制备金属钛的示意图。
请回答下列问题:
(1)写出甲装置中碳棒表面的电极反应式:_________________________
(2)已知:5Cl2+I2+6H2O=10HCl+2HIO3。若将湿润的淀粉KI试纸置于乙装置中的碳棒附近,现象为________________________________;若乙装置中转移0.02 mol电子后停止实验,烧杯中溶液的体积为200 mL,则此时溶液的pH=________。(室温条件下,且不考虑电解产物的相互反应)
(3)工业上经常用到离子交换膜,离子交换膜有阳离子交换膜和阴离子交换膜两种,阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过。当乙装置中的反应用于工业生产时,为了阻止两极产物之间的反应,通常用如丙图所示的装置,Na+的移动方向如图中标注,则H2的出口是________(填“C”、“D”、“E”或“F”);________(填“能”或“不能”)将阳离子交换膜换成阴离子交换膜。
(4)研究发现,可以用石墨作阳极、钛网作阴极、熔融CaO作电解质,利用丁装置获得金属钙,并以钙为还原剂,还原二氧化钛制备金属钛。
①写出阳极的电极反应式:_____________________________________。
②在制备金属钛前后,CaO的总量不变,其原因是(请结合化学用语解释)____________________________________ __。
③电解过程中需定期更换阳极材料的原因是
___________________ __________________________________________
乙醇汽油是一种由粮食及各种植物纤维加工成的燃料乙醇和普通汽油按一定比例混配形成的新型替代能源。按照我国的国家标准,乙醇汽油是用90%的普通汽油与10%的乙醇调和而成。
(1)由粮食或各种植物纤维可得到葡萄糖,写出葡萄糖制得乙醇的化学方程式: 。
(2)在常温常压下,1gC2H5OH完全燃烧生成CO2和液态H2O时放出29.71 kJ热量,表示该反应的热化学方程式为 。
(3)下图是一个乙醇燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题:

①加入乙醇的Pt电极的电极反应式为_________________________。
②在工作过程中,乙池中两电极均收集到标准状况下224mL气体时,甲池中理论上消耗氧气的体积为 mL(标准状况下);若此时乙池溶液体积为200mL,则乙池中溶液的pH为 。
③若要使②中乙池的溶液完全恢复到起始状态,可向乙池中加入 (填代号)
A.0.01molCu
B.0.01molCuO
C.0.01molCu(OH)2
D.0.01molCuCO3
E.0.01molCuSO4
F.0.005molCu2(OH)2CO3
乙醇汽油是一种由粮食及各种植物纤维加工成的燃料乙醇,和普通汽油按一定比例混配形成的新型替代能源。有人指出,近年来冬季北方路面经常结冰,是由于大量使用乙醇汽油,而乙醇燃烧时,会产生比普通汽油更多的水的原因导致的。某校研究性学习小组设计了如下实验,测定学校附近加油站的93号汽油中乙醇的含量,并比较乙醇燃烧与普通汽油燃烧产生水的量。
甲同学认为,分离互溶的液体混合物最好的方法就是蒸馏,只要通过蒸馏并收集乙醇汽油中的乙醇就可以计算其含量。于是,他设计了按下图装置进行的蒸馏实验,

⑴请找出上图装置中的两处错误: , 。
经查阅相关资料得到乙醇及普通汽油主要成分(5—11碳的烷烃)的沸点如下表:
|
有机物 |
乙醇 |
戊烷 |
己烷 |
庚烷 |
辛烷 |
壬烷 |
癸烷 |
十一烷 |
|
沸点/℃ |
78.4 |
36.1 |
68.7 |
98.5 |
125.8 |
150.8 |
174.1 |
195.6 |
⑵乙同学根据上表中的数据提出,甲同学的方案不易实施,得不到纯净的乙醇,请简述其中的原因: 。
⑶乙同学根据查阅的资料提出:可以用水萃取乙醇汽油中的乙醇,以此实现分离乙醇的目的。向分液漏斗中加入乙醇汽油和蒸馏水,如想使乙醇全部进入水层需要进行的操作是: ;静置分层后普通汽油在 层(填“上”或“下”)。通过测定普通汽油的质量与原乙醇汽油的质量就可计算出乙醇的质量分数。
⑷燃烧时产生水的多少是由有机物的含氢量(氢元素的质量分数)决定的,根据上表中普通汽油的成分可知,普通汽油中含氢量最高的是: (填分子式)、最低的是: (填分子式);则等质量的乙醇与这两种有机物相比较,完全燃烧时产生水的质量最小的
是: (填分子式)。
乙醇汽油是一种由粮食及各种植物纤维加工成的燃料乙醇和普通汽油按一定比例混配形成的新型替代能源。按照我国的国家标准,乙醇汽油是用90%的普通汽油与10%的乙醇调和而成。
(1)由粮食或各种植物纤维可得到葡萄糖,写出葡萄糖制得乙醇的化学方程式: 。
(2)在常温常压下,1gC2H5OH完全燃烧生成CO2和液态H2O时放出29.71 kJ热量,表示该反应的热化学方程式为 。
(3)下图是一个乙醇燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题: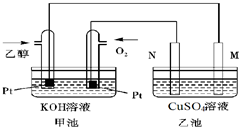
①加入乙醇的Pt电极的电极反应式为_________________________。
②在工作过程中,乙池中两电极均收集到标准状况下224mL气体时,甲池中理论上消耗氧气的体积为 mL(标准状况下);若此时乙池溶液体积为200mL,则乙池中溶液的pH为 。
③若要使②中乙池的溶液完全恢复到起始状态,可向乙池中加入 (填代号)
| A.0.01molCu |
| B.0.01molCuO |
| C.0.01molCu(OH)2 |
| D.0.01molCuCO3 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com