
ĢāÄæĮŠ±ķ(°üĄØ“š°øŗĶ½āĪö)
£Ø±¾Ģā16·Ö£©½µµĶ“óĘųÖŠCO2µÄŗ¬ĮæŗĶÓŠŠ§µŲæŖ·¢ĄūÓĆCO2Õż³ÉĪŖŃŠ¾æµÄÖ÷ŅŖæĪĢā”£
£Ø1£©ŅŃÖŖŌŚ³£ĪĀ³£Ń¹ĻĀ£ŗ
¢Ł 2CH3OH(l) £« 3O2(g) £½ 2CO2(g) £« 4H2O(g) ¦¤H £½£1275.6 kJ/mol
¢Ś 2CO (g)+ O2(g) £½ 2CO2(g) ¦¤H £½£566.0 kJ/mol
¢Ū H2O(g) £½ H2O(l) ¦¤H £½£44.0 kJ/mol
Š“³ö¼×“¼²»ĶźČ«Č¼ÉÕÉś³ÉŅ»Ńõ»ÆĢ¼ŗĶŅŗĢ¬Ė®µÄČČ»Æѧ·½³ĢŹ½£ŗ ”£
£Ø2£©ŌŚČŻ»żĪŖ2LµÄĆܱÕČŻĘ÷ÖŠ£¬³äČė2mol CO2ŗĶ6mol H2£¬ŌŚĪĀ¶Č500”ꏱ·¢Éś·“Ó¦£ŗ
CO2£Øg£©+ 3H2£Øg£© CH3OH£Øg£©+ H2O£Øg£© ”÷H<0”£CH3OHµÄÅضČĖꏱ¼ä±ä»ÆČēĶ¼”£»Ų“šÓŠ¹ŲĪŹĢā£ŗ
CH3OH£Øg£©+ H2O£Øg£© ”÷H<0”£CH3OHµÄÅضČĖꏱ¼ä±ä»ÆČēĶ¼”£»Ų“šÓŠ¹ŲĪŹĢā£ŗ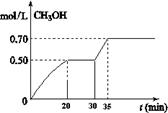
¢Ł“Ó·“Ó¦æŖŹ¼µ½20·ÖÖÓŹ±£¬H2µÄĘ½¾ł·“Ó¦ĖŁĀŹv(H2)£½_________________”£
¢Ś“Ó30·ÖÖÓµ½35·ÖÖÓ“ļµ½ŠĀµÄĘ½ŗā£¬øıäµÄĢõ¼žæÉÄÜŹĒ ”£
A. Ōö“óŃ¹Ēæ B.¼ÓČė“߻ƼĮ C.ÉżøßĪĀ¶Č D.Ōö“ó·“Ó¦ĪļµÄÅضČ
¢ŪĮŠŹ½¼ĘĖćøĆ·“Ó¦ŌŚ35·ÖÖÓ“ļµ½ŠĀĘ½ŗāŹ±µÄĘ½ŗā³£Źż(±£Įō2Ī»Š”Źż)
¢ÜČē¹ūŌŚ30·ÖÖÓŹ±,ŌŁĻņČŻĘ÷ÖŠ³äČė2mol CO2ŗĶ6mol H2£¬±£³ÖĪĀ¶Č²»±ä£¬“ļµ½ŠĀĘ½ŗāŹ±£¬CH3OHµÄÅضČ____________1mol.L-1(Ģī”°>”±”¢”°<”±»ņ”°=”±)”£
£Ø3£©Ņ»ÖÖŌµē³ŲµÄ¹¤×÷ŌĄķĪŖ£ŗ2Na2S2 + NaBr3  Na2S4 + 3NaBr”£ÓĆøƵē³ŲĪŖµēŌ“£¬ŅŌĒāŃõ»Æ¼ŲĖ®ČÜŅŗ×÷µē½āÖŹ½ųŠŠµē½ā£¬Ź¹CO2ŌŚĶµē¼«ÉĻæÉ×Ŗ»ÆĪŖ¼×Ķ锣
Na2S4 + 3NaBr”£ÓĆøƵē³ŲĪŖµēŌ“£¬ŅŌĒāŃõ»Æ¼ŲĖ®ČÜŅŗ×÷µē½āÖŹ½ųŠŠµē½ā£¬Ź¹CO2ŌŚĶµē¼«ÉĻæÉ×Ŗ»ÆĪŖ¼×Ķ锣
¢ŁøƵē³Ųøŗ¼«µÄµē¼«·“Ó¦Ź½ĪŖ£ŗ ”£
¢Śµē½ā³ŲÖŠ²śÉśCH4Ņ»¼«µÄµē¼«·“Ó¦Ź½ĪŖ£ŗ ”£
£Ø4£©ĻĀĶ¼ŹĒNaOHĪüŹÕCO2ŗóijÖÖ²śĪļµÄĖ®ČÜŅŗŌŚpH“Ó0ÖĮ14µÄ·¶Ī§ÄŚH2CO3”¢HCO3£”¢CO32£ČżÖֳɷÖĘ½ŗāŹ±µÄ×é³É·ÖŹż”£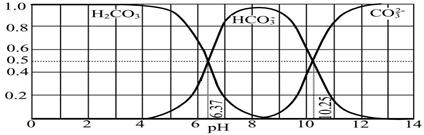
ĻĀĮŠŠšŹöÕżČ·µÄŹĒ ”£
A£®“ĖĶ¼ŹĒ1.0 mol”¤L-1Ģ¼ĖįÄĘČÜŅŗµĪ¶Ø1.0 mol”¤L-1 HClČÜŅŗµÄµĪ¶ØĒśĻß
B£®ŌŚpH·Ö±šĪŖ6.37¼°10.25Ź±£¬ČÜŅŗÖŠc(H2CO3)=c(HCO3£)=c(CO32£)
C£®ČĖĢåŃŖŅŗµÄpHŌ¼ĪŖ7.4£¬ŌņCO2ŌŚŃŖŅŗÖŠ¶ąŅŌHCO3£ŠĪŹ½“ęŌŚ
D£®ČōÓĆCO2ŗĶNaOH·“Ó¦ÖĘČ”NaHCO3£¬ŅĖæŲÖĘČÜŅŗµÄpHĪŖ7”«9Ö®¼ä
 CH3OH£Øg£©+ H2O£Øg£© ”÷H<0”£CH3OHµÄÅضČĖꏱ¼ä±ä»ÆČēĶ¼”£»Ų“šÓŠ¹ŲĪŹĢā£ŗ
CH3OH£Øg£©+ H2O£Øg£© ”÷H<0”£CH3OHµÄÅضČĖꏱ¼ä±ä»ÆČēĶ¼”£»Ų“šÓŠ¹ŲĪŹĢā£ŗ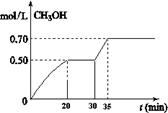
 Na2S4 + 3NaBr”£ÓĆøƵē³ŲĪŖµēŌ“£¬ŅŌĒāŃõ»Æ¼ŲĖ®ČÜŅŗ×÷µē½āÖŹ½ųŠŠµē½ā£¬Ź¹CO2ŌŚĶµē¼«ÉĻæÉ×Ŗ»ÆĪŖ¼×Ķ锣
Na2S4 + 3NaBr”£ÓĆøƵē³ŲĪŖµēŌ“£¬ŅŌĒāŃõ»Æ¼ŲĖ®ČÜŅŗ×÷µē½āÖŹ½ųŠŠµē½ā£¬Ź¹CO2ŌŚĶµē¼«ÉĻæÉ×Ŗ»ÆĪŖ¼×Ķ锣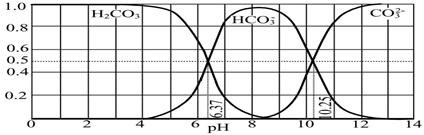
| ĪĀ¶Č | 250”ę | 300”ę | 350”ę |
| K | 2.041 | 0.270 | 0.012 |
 £Ø2012?Ģ«ŌŅ»Ä££©A”«JŹĒ֊ѧ»Æѧ֊³£¼ūµÄ¼øÖÖĪļÖŹ£¬ĖüĆĒÖ®¼äµÄ×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾£Ø²æ·Ö·“Ó¦Ģõ¼žŅŃĀŌČ„£©£®ŅŃÖŖ³£ĪĀĻĀAĪŖ¹ĢĢåµ„ÖŹ£¬BĪŖµ»ĘÉ«·ŪÄ©£¬C”¢F”¢IĪŖĘųĢ¬µ„ÖŹ£¬EŌŚ³£ĪĀĻĀĪŖŅŗĢ壬JæÉÓĆ×÷ɱ¾śĻū¶¾¼Į£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø2012?Ģ«ŌŅ»Ä££©A”«JŹĒ֊ѧ»Æѧ֊³£¼ūµÄ¼øÖÖĪļÖŹ£¬ĖüĆĒÖ®¼äµÄ×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾£Ø²æ·Ö·“Ó¦Ģõ¼žŅŃĀŌČ„£©£®ŅŃÖŖ³£ĪĀĻĀAĪŖ¹ĢĢåµ„ÖŹ£¬BĪŖµ»ĘÉ«·ŪÄ©£¬C”¢F”¢IĪŖĘųĢ¬µ„ÖŹ£¬EŌŚ³£ĪĀĻĀĪŖŅŗĢ壬JæÉÓĆ×÷ɱ¾śĻū¶¾¼Į£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ

| 4b |
| a |
| 4b |
| a |
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com