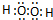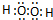(2009?清远模拟)德国人哈伯在1909年发明的合成氨反应原理为:N
2(g)+3H
2(g)?2NH
3(g) 已知298K时:△H=-92.4kJ?mol
-1试回答下列问题:
(1)在298K时,将10mol N
2和30mol H
2放入合成塔中,为何放出的热量小于924kJ?
该反应为可逆反应,10molN2和30molH2不可能完全反应,所以放出的热量小于10×10×92.4kJ=924kJ
该反应为可逆反应,10molN2和30molH2不可能完全反应,所以放出的热量小于10×10×92.4kJ=924kJ
.
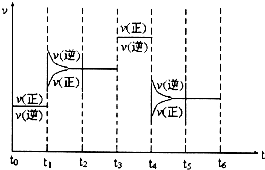
(2)如图一在一定条件下,将1mol N
2与3mol H
2混合于一个10L密闭容器中,反应达到A平衡时,混合气体中氨占25%,试回答:
①N
2的转化率α
A为
40%
40%
.
②在状态A时,平衡常数K
A=
(代入数值的表达式,不写出具体数值)当温度由T
1变化到T
2时,K
A>
>
K
B(填“>”、“<”或“=”)
(3)图二是实验室模拟工业法合成氨的简易装置.简述检验有氨气生成的方法
用湿润的红色石蕊试纸放在导管口处,若试纸变蓝,说明有氨气生成
用湿润的红色石蕊试纸放在导管口处,若试纸变蓝,说明有氨气生成
.在1998年希腊亚里斯多德大学的Marmellos和Stoukides采用高质子导电性的SCY陶瓷(能传递H
+),实现了高温常压下高转化率的电化学合成氨.其实验装置如图.阴极的电极反应式
N2+6e-+6H+=2NH3
N2+6e-+6H+=2NH3
.

 (2009?清远模拟)德国人哈伯在1909年发明的合成氨反应原理为:N2(g)+3H2(g)?2NH3(g) 已知298K时:△H=-92.4kJ?mol-1试回答下列问题:
(2009?清远模拟)德国人哈伯在1909年发明的合成氨反应原理为:N2(g)+3H2(g)?2NH3(g) 已知298K时:△H=-92.4kJ?mol-1试回答下列问题: 已知298K时:
已知298K时: