
题目列表(包括答案和解析)
(每空3分,共12分)一定条件下,在体积为3 L的密闭容器中,一氧化碳与氢气反应生成甲醇:CO(g)+2H2(g) CH3OH(g)根据题意完成下列各题:
CH3OH(g)根据题意完成下列各题:
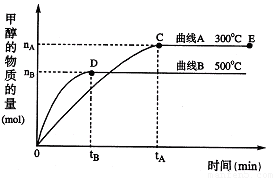
(1)在500℃,从反应开始到刚好达到平衡,氢气的平均反应速率ν(H2)= (用图中相应字母表示)
(2)在其他条件不变的情况下,将处于E点的体系的体积压缩到原来的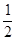 ,下列有关该体系的说法正确的是
(填序号)
,下列有关该体系的说法正确的是
(填序号)
a 氢气的浓度减少 b 正反应速率加快,逆反应速率变慢,平衡正向移动
c 甲醇的物质的量增加 d 重新平衡时c(CO)/c(CH3OH)增大
(3)从反应的方向判断,正向进行的反应 (填序号:A. 高温时 B.低温时 C.任何温度都能 D.任何温度都不能)自发进行。
(4)在不改变反应物用量的情况下,提高CO的转化率采取的措施是
(答两点即可)
(12分) A、J是日常生活中常见的两种金属,这两种金属和NaOH组成原电池,A作负极;F常温下是气体,各物质有以下的转化关系(部分产物及条件略去)。
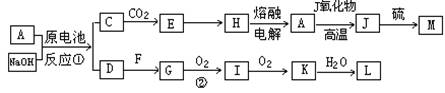
请回答以下问题:
(1)写出原电池的负极反应方程式______________________________________。
(2)常温时pH=12的C溶液中,溶质的阳离子与溶质的阴离子浓度之差为____________(写出计算式);相同条件下,等浓度的C溶液与CH3COONa溶液中,C的阴离子与CH3COO-浓度的大小关系:前者_______后者(用“>”、“<”或“=”表示)。
(3)写出②的化学方程式____________________________________________________。
(4)含A元素的某盐X常做净水剂,X做焰色反应时,透过钴玻璃观察火焰呈紫色。
①X的水溶液与NaHCO3溶液混合,反应的离子方程式为 。
②500mLX的溶液与Ba(OH)2反应生成沉淀的质量与加入Ba(OH)2物质的量的关系如图:
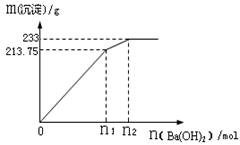
请回答:X晶体的俗名为__________;其溶液的物质的量浓度为_________mol/L。
(每空3分,共12分)一定条件下,在体积为3 L的密闭容器中,一氧化碳与氢气反应生成甲醇:CO(g)+2H2(g)CH3OH(g)根据题意完成下列各题:
(1)在500℃,从反应开始到刚好达到平衡,氢气的平均反应速率ν(H2)= (用图中相应字母表示)
(2)在其他条件不变的情况下,将处于E点的体系的体积压缩到原来的![]() ,下列有关该体系的说法正确的是 (填序号)
,下列有关该体系的说法正确的是 (填序号)
a 氢气的浓度减少 b 正反应速率加快,逆反应速率变慢,平衡正向移动
c 甲醇的物质的量增加 d 重新平衡时c(CO)/c(CH3OH)增大
(3)从反应的方向判断,正向进行的反应 (填序号:A. 高温时 B.低温时 C.任何温度都能 D.任何温度都不能)自发进行。
(4)在不改变反应物用量的情况下,提高CO的转化率采取的措施是
(答两点即可)
(12分) A、J是日常生活中常见的两种金属,这两种金属和NaOH组成原电池,A作负极;F常温下是气体,各物质有以下的转化关系(部分产物及条件略去)。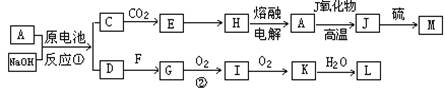
请回答以下问题:
(1)写出原电池的负极反应方程式______________________________________。
(2)常温时pH=12的C溶液中,溶质的阳离子与溶质的阴离子浓度之差为____________(写出计算式);相同条件下,等浓度的C溶液与CH3COONa溶液中,C的阴离子与CH3COO-浓度的大小关系:前者_______后者(用“>”、“<”或“=”表示)。
(3)写出②的化学方程式____________________________________________________。
(4)含A元素的某盐X常做净水剂,X做焰色反应时,透过钴玻璃观察火焰呈紫色。
①X的水溶液与NaHCO3溶液混合,反应的离子方程式为 。
②500mLX的溶液与Ba(OH)2反应生成沉淀的质量与加入Ba(OH)2物质的量的关系如图:
请回答:X晶体的俗名为__________;其溶液的物质的量浓度为_________mol/L。
(12分) A、J是日常生活中常见的两种金属,这两种金属和NaOH组成原电池,A作负极;F常温下是气体,各物质有以下的转化关系(部分产物及条件略去)。
请回答以下问题:
(1)写出原电池的负极反应方程式______________________________________。
(2)常温时pH=12的C溶液中,溶质的阳离子与溶质的阴离子浓度之差为____________(写出计算式);相同条件下,等浓度的C溶液与CH3COONa溶液中,C的阴离子与CH3COO-浓度的大小关系:前者_______后者(用“>”、“<”或“=”表示)。
(3)写出②的化学方程式____________________________________________________。
(4)含A元素的某盐X常做净水剂,X做焰色反应时,透过钴玻璃观察火焰呈紫色。
①X的水溶液与NaHCO3溶液混合,反应的离子方程式为 。
②500mLX的溶液与Ba(OH)2反应生成沉淀的质量与加入Ba(OH)2物质的量的关系如图:
请回答:X晶体的俗名为__________;其溶液的物质的量浓度为_________mol/L。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com