
题目列表(包括答案和解析)
实验室要配制100mL 0.1mol?L-1的NaCl溶液,试回答下列各题:
(1)下列仪器中,不会用到的是
A.锥形瓶 B.200mL容量瓶 C.量筒 D.胶头滴管 E.100mL容量瓶 F.天平
(2)若要实施配制,除上述仪器外,尚缺的仪器或用品是_____________________。
(3)容量瓶上除有刻度线外还应标有___________,在使用前必须检查容量瓶是否完好以及________________处是否漏水。(填容量瓶的受检部位)
(4)人们常将配制过程简述为以下各步骤:
A.冷却 B.称量 C.洗涤 D.定容 E.溶解 F.摇匀 G.移液
其正确的操作顺序应是_____________________(填各步骤序号)。
(5)配制完毕后,教师指出有四位同学各进行了下列某一项错误操作,你认为这四项错误操作会导致所得溶液浓度偏高的是
A.定容时仰视容量瓶刻度线
B.定容时俯视容量瓶刻度线
C.将溶解冷却的溶液转入容量瓶后就直接转入定容操作
D.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处
(6)通过计算可得出可用托盘天平称取NaCl固体______________克。若用4mol/L的NaCl溶液配制应用量筒量取________________mL该溶液。

| 实验编号 | 样品和辅助试剂 | 消耗盐酸体积(mL) |
| 1 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 33.45 |
| 2 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 33.55 |
| 3 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 33.50 |
| 4 | 10.00mL蒸馏水、0.2g催化剂、20mL浓硫酸 | 1.50 |


(一)测定目的:测定××牌软包装橙汁维生素C含量。
(二)测定原理:C6H8O6+I![]() C6H6O6+2H++2I-。
C6H6O6+2H++2I-。
(三)实验用品及试剂:
(1)仪器和用品:(自选,略)。
(2)试剂:指示剂_________(填名称)、浓度为7.50×10-3 mol·L-1标准碘溶液、蒸馏水等。
(四)实验过程:
(1)洗涤仪器,检查滴定管是否漏液,润洗后装好标准碘溶液待用。
(2)打开橙汁包装,目测:颜色——橙黄色,澄清度——好,用_________ (填仪器名称)向锥形瓶中移入20.00 mL待测橙汁,滴入2滴指示剂。
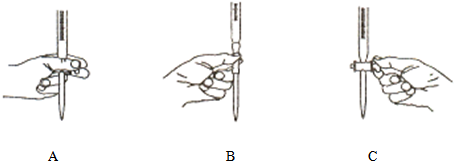
(3)用左手控制滴定管的_________(填部位),右手摇动锥形瓶,眼睛注视_________,直到滴定终点,滴定到终点的现象是_________。
(五)数据记录与处理,若经数据处理,滴定中消耗标准碘溶液的体积是15.00 mL,则此橙汁中维生素C的含量是_________mg·L-1。
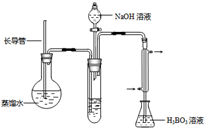 ④取下锥形瓶,滴加指示剂,用0.1000mol?L-1盐酸标准液滴定;
④取下锥形瓶,滴加指示剂,用0.1000mol?L-1盐酸标准液滴定;| 实验编号 | 样品和辅助试剂 | 消耗盐酸体积(mL) |
| 1 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 33.45 |
| 2 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 33.55 |
| 3 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 33.50 |
| 4 | 10.00mL蒸馏水、0.2g催化剂、20mL浓硫酸 | 1.50 |

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com