
题目列表(包括答案和解析)
某研究性学习小组在网上收集到如下信息:钾、钙、钠、镁等活泼金属都能在CO2气体中燃烧。他们对钠在CO2气体中燃烧后的产物中的白色物质进行了如下探究:
【实验】将燃烧的钠迅速伸入到盛有装满CO2的集气瓶中,钠在其中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上粘附着白色物质。
【提出假设】假设1:白色物质是Na2O, 假设2:白色物质是Na2CO3。
假设3:
【设计实验方案.验证假设】该小组对燃烧后的白色产物进行如下探究:
| 实验方案 | 实验操作 | 实验现象 | 结论 |
| 方案1 | 取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液 | 溶液变成红色 | 白色物质为Na2O |
| 方案2 | ①取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的CaCl2溶液 | 出现白色沉淀 | |
| ③静置片刻,取上层清液于试管中,滴加无色酚酞试液 | 无明显现象 |
【思考与交流】
(1)甲同学认为方案1得到的结论不正确,其理由是 。
(2)乙同学认为方案2得到的结论正确,白色物质为 。
(3)通过方案1和方案2的实验,你认为上述三个假设中, 成立。你的理由是 。
(4)钠在二氧化碳中燃烧的化学方程式为
(5)丙同学认为白色物质有可能是氢氧化钠。你是否同意丙同学的观点,并简述理由:
22.(8分)某化学研究性学习小组探究Fe3+和SO32-之间发生的反应。
(1)取5mLFeCl3浓溶液于试管中,逐滴加入Na2SO3浓溶液,观察到溶液颜色由黄色变为红棕色,继续加入Na2SO3浓溶液至过量,溶液颜色加深,最终变为红褐色。无气泡产生,无沉淀生成。这种红褐色液体是___________________。
(2)除了观察到以上的现象外,有成员提出了另一种可能:发生氧化还原反应。反应的离子方程式为 。
研究性学习小组设计了两种实验方案证明发生了氧化还原反应。请把实验方案补充完整:
方案一:检验溶液中含有Fe2+证明发生了氧化还原反应
方案二:检验溶液中含有 证明发生了氧化还原反应
实验用品:0.1mol/L BaCl2、3mol/L盐酸、0.1mol/LKMnO4(H+)、氯水、20%KSCN、0.5mol/LKI;试管若干、胶头滴管若干
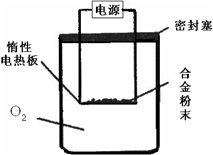
Ⅰ预处理:将(1)中获得的混合物放在如右图装置中处理足够时间。
 Ⅱ检验过程
Ⅱ检验过程
| 操作 | 现象及结论 |
| 基于方案一: | |
| 基于方案二: |

某校化学兴趣小组的同学在进行研究性学习时,对“NO2能否支持燃烧”这个问题很感兴趣,他们决定自己动手设计实验进行探究。

(1)甲组同学设计的实验方案:向烧瓶中加入适量浓硝酸并加热,当烧瓶中有红棕色气体产生之后,将燃着的木条伸入烧瓶中,发现木条火焰熄灭。由此他们得出“NO2不能支持燃烧”的结论。
甲组同学所得的结论一定正确吗?请你说明理由:
。
(2)乙组同学通过查阅资料得知,一些不活泼金属的硝酸盐受热时也能产生NO2气体,如:2Cu(NO3)2![]() 2CuO+4NO2↑+O2↑,2AgNO3
2CuO+4NO2↑+O2↑,2AgNO3![]() 2Ag+2NO2↑+O2↑。他们根据此原理设计了如右图所示的实验装置(加热、夹持仪器未画出),并分别用Cu(NO3)2和AgNO3进行实验,实验中发现当红棕色气体进入集气瓶后,带火星的木炭均能复燃,乙组同学由此得出“NO2能支持燃烧”的结论。
2Ag+2NO2↑+O2↑。他们根据此原理设计了如右图所示的实验装置(加热、夹持仪器未画出),并分别用Cu(NO3)2和AgNO3进行实验,实验中发现当红棕色气体进入集气瓶后,带火星的木炭均能复燃,乙组同学由此得出“NO2能支持燃烧”的结论。
①老师认为上述两个实验中,有一个实验所得结论是不可靠的,你认为该实验中选用的反应物是 ,其结论不可靠的原因是 。
②运用该实验装置进行实验时,造成的不良后果是 。
(3)丙组同学拟设计一个用较为纯净的NO2气体(无O2产生)来探究“NO2能否支持燃烧”的实验。

①丙组同学制取NO2的化学方程式是 。
②如图是该组同学设计的制取并收集NO2气体的实验装置,请在方框中将该装置补充完整,并注明补充装置中所用试剂。
 测定剩余固体质量
测定剩余固体质量 测定生成气体的体积实验装置:
测定生成气体的体积实验装置: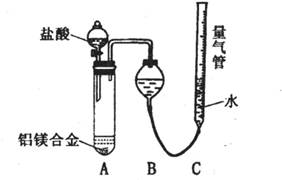
 问题讨论:
问题讨论: 测定剩余固体质量
测定剩余固体质量 测定生成气体的体积实验装置:
测定生成气体的体积实验装置:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com